Publicado el: 05/08/2014
Autor/es: Dra Mabel E. Vázquez FCAyF - UNLP (Argentina)
Ver más
INTRODUCCIÓN
El calcio (Ca) y magnesio (Mg) son requeridos para el crecimiento vegetal en cantidades relativamente grandes, aunque inferiores al nitrógeno (N), fósforo (P) y potasio (K). No existe en Argentina, sin embargo, tradición en su empleo como fertilizantes en cultivos extensivos, particularmente en ámbitos templados. Esto se debe a que los suelos de estas regiones poseen, mayoritariamente, cantidades naturales elevadas de los mismos, debido al tipo de materiales originales y el moderado grado de meteorización. Sin embargo, en algunas regiones templadas el proceso de acidificación y disminución o desbalance del contenido de estos nutrientes en el suelo, se ha producido fundamentalmente por razones antrópicas. La causa principal del proceso de su pérdida es la exportación de bases a través de la producción agrícola y ganadera. Esto ocurrió durante largos periodos de tiempo, a veces superiores a la centuria, en regiones donde no ha existido historia de reposición de estos nutrientes. Otra de las razones de la acidificación en estos suelos ha sido el importante crecimiento en la últimas décadas del uso de fertilizantes de alto índice de acidez, fundamentalmente los nitrogenados amoniacales o con grupo amino como la urea. En estas situaciones se han informado respuestas por parte de numerosos cultivos a la aplicación de fertilizantes cálcicos y magnésicos en condiciones experimentales, así como también a la aplicación de enmiendas básicas tendientes a neutralizar la acidez del suelo. En producciones intensivas, aun existiendo cantidades adecuadas de Ca y Mg en el suelo, puede ocurrir que el elevado ritmo de la demanda por parte de este tipo de cultivos provoque que no se logren reponer estos nutrientes a la solución del suelo a la velocidad con que son absorbidos, por lo que en muchas situaciones es necesaria también su aplicación para evitar severos daños en los frutos.
El calcio (Ca) y magnesio (Mg) son requeridos para el crecimiento vegetal en cantidades relativamente grandes, aunque inferiores al nitrógeno (N), fósforo (P) y potasio (K). No existe en Argentina, sin embargo, tradición en su empleo como fertilizantes en cultivos extensivos, particularmente en ámbitos templados. Esto se debe a que los suelos de estas regiones poseen, mayoritariamente, cantidades naturales elevadas de los mismos, debido al tipo de materiales originales y el moderado grado de meteorización. Sin embargo, en algunas regiones templadas el proceso de acidificación y disminución o desbalance del contenido de estos nutrientes en el suelo, se ha producido fundamentalmente por razones antrópicas. La causa principal del proceso de su pérdida es la exportación de bases a través de la producción agrícola y ganadera. Esto ocurrió durante largos periodos de tiempo, a veces superiores a la centuria, en regiones donde no ha existido historia de reposición de estos nutrientes. Otra de las razones de la acidificación en estos suelos ha sido el importante crecimiento en la últimas décadas del uso de fertilizantes de alto índice de acidez, fundamentalmente los nitrogenados amoniacales o con grupo amino como la urea. En estas situaciones se han informado respuestas por parte de numerosos cultivos a la aplicación de fertilizantes cálcicos y magnésicos en condiciones experimentales, así como también a la aplicación de enmiendas básicas tendientes a neutralizar la acidez del suelo. En producciones intensivas, aun existiendo cantidades adecuadas de Ca y Mg en el suelo, puede ocurrir que el elevado ritmo de la demanda por parte de este tipo de cultivos provoque que no se logren reponer estos nutrientes a la solución del suelo a la velocidad con que son absorbidos, por lo que en muchas situaciones es necesaria también su aplicación para evitar severos daños en los frutos.
REQUERIMIENTOS DE LOS CULTIVOS, FUNCIONES FISIOLÓGICAS Y SÍNTOMAS DE DEFICIENCIA
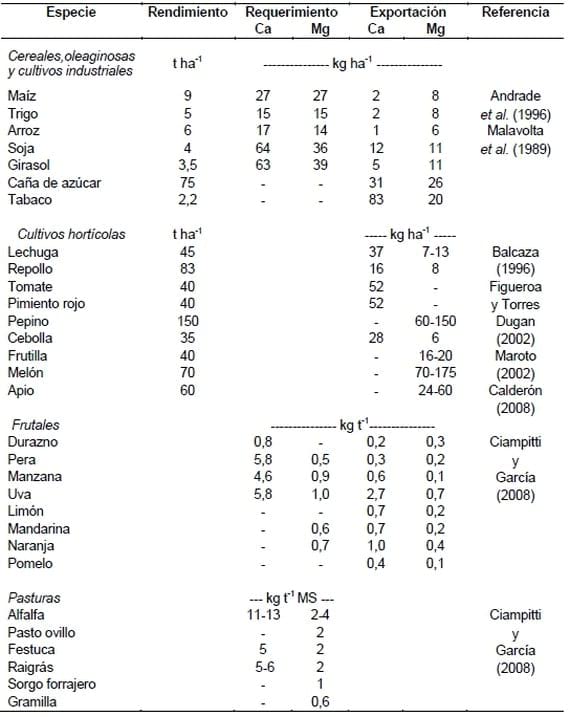
Los requerimientos y/o exportación de Ca y Mg de diferentes cultivos se muestran en la Tabla 1. Los valores de exportación de estos nutrientes son sumamente variables, alcanzando cifras cercanas a 200 kg ha-1 en el caso de Ca y 50 kg ha-1 en el de Mg, dependiendo de la especie y los rendimientos. La producción hortícola es sumamente exigente en estos elementos y es en suelos bajo este tipo de producción donde generalmente se informan los balances más negativos. En un estudio realizado por Balcaza (2003), se evaluó la evolución del Ca intercambiable en suelos de invernáculos del Gran La Plata y se informó una disminución de 12,8 a 7,1 cmolc kg-1 de Ca, en 12 años de producción.
Los requerimientos y/o exportación de Ca y Mg de diferentes cultivos se muestran en la Tabla 1. Los valores de exportación de estos nutrientes son sumamente variables, alcanzando cifras cercanas a 200 kg ha-1 en el caso de Ca y 50 kg ha-1 en el de Mg, dependiendo de la especie y los rendimientos. La producción hortícola es sumamente exigente en estos elementos y es en suelos bajo este tipo de producción donde generalmente se informan los balances más negativos. En un estudio realizado por Balcaza (2003), se evaluó la evolución del Ca intercambiable en suelos de invernáculos del Gran La Plata y se informó una disminución de 12,8 a 7,1 cmolc kg-1 de Ca, en 12 años de producción.
Tabla 1. Requerimientos y/o exportación de Ca y Mg para diferentes cultivos.
Una gran proporción del Ca vegetal se encuentra formando parte de las paredes celulares, como oxalato de Ca y otros ácidos orgánicos en el apoplasma o las vacuolas. Dentro de sus principales funciones puede citarse el mantenimiento de la integridad de las membranas, la estabilidad de las paredes celulares, el gravitropismo de raíces y tallos, la deposición de callosa y la regulación de varias enzimas, entre ellas ?-amilasa, proteino quinasas y ATP-asas.
Los síntomas de deficiencia de Ca en las plantas generalmente se concentran en tejidos meristemáticos (áreas de activo crecimiento y división celular) de hojas, tallos y raíces. Esto se debe a la relativamente baja movilidad de este elemento dentro de la planta, lo que determina una reducida tasa de removilización hacia tejidos jóvenes de rápido crecimiento (Azcon Bieto y Talon, 2008). La deficiencia de Ca causa deformaciones en los tejidos y muerte de los puntos de crecimiento incluyendo yemas, flores y puntas de raíces. Los ápices y márgenes de las hojas se tornan cloróticos y/o necróticos. Las leguminosas deficientes en Ca presentan un escaso desarrollo radical con reducida capacidad de fijación de N (nódulos blancos). La baja tasa de absorción de Ca+2 combinada con una limitada translocación de carbohidratos puede causar distintos síntomas en frutos y vegetales. Ejemplos de estos síntomas son la enfermedad llamada podredumbre apical (blossom end rot) en tomate y pimiento, deformaciones en melón, producción de sabor amargo en manzano (bitter pit), mancha marrón en el interior del fruto de tomate, corazón negro en maní y ajo, y ahuecamiento en zanahoria, entre otras.
La función fisiológica de mayor trascendencia del Mg es la de formar parte de la molécula de clorofila, aunque no es el destino más importante desde el punto de vista cuantitativo, ya que sólo del 15 al 20% del Mg en el vegetal está ligado a la clorofila. El resto se encuentra localizado en forma iónica soluble en el espacio intratilacoidal y al iluminarse el cloroplasto pasa al estroma, donde activa enzimas como la rubisco, la fosfo-enolpiruvato carboxilasa y la glutamato sintasa. La asignación fotosintética del C y el N, depende en gran medida, de la concentración de Mg en el cloroplasto (Azcon Bieto y Talon, 2008). Cuando una planta es deficiente en Mg, disminuye el N proteico y aumenta el no proteico, por su efecto sobre las partículas ribosomales. Este hecho permite utilizar la medida del N no proteico soluble como índice de la deficiencia de Mg. Una sustancial proporción de este elemento está involucrada en la regulación del pH celular y el balance catión-anión. El Mg también interviene en el metabolismo energético de la planta al formar complejos con el ATP, estos permiten la fosforilación del ADP para transformarse en ATP. Si bien los síntomas de deficiencia de Mg varían de una especie a otra, existen algunas características generales que pueden citarse. A diferencia del Ca, los síntomas de deficiencia de Mg se concentran en las hojas inferiores debido a la alta movilidad de este nutriente dentro de las plantas, lo que determina una activa migración ante situaciones de deficiencia. Se producen clorosis internervales a causa de la menor fotosíntesis y acumulación de carbohidratos, ya que las células del mesófilo próximas a la nervadura conservan la clorofila por más tiempo. Finalmente, puede producirse necrosis en los casos más severos, empezando por las hojas maduras y avanzando hacia las más nuevas, a causa de su retranslocación vía floema. Las hojas se tornan rígidas y quebradizas, y suelen caer prematuramente. En el caso de los cereales, la base de las hojas muestra pequeñas manchas verde oscuro que se destacan sobre el resto del limbo, verde pálido amarillento. Finalmente se necrosan las puntas de las hojas. Los órganos de almacenamiento, tales como tubérculos o granos de cereales, pueden acumular menores cantidades de carbohidratos.
La función fisiológica de mayor trascendencia del Mg es la de formar parte de la molécula de clorofila, aunque no es el destino más importante desde el punto de vista cuantitativo, ya que sólo del 15 al 20% del Mg en el vegetal está ligado a la clorofila. El resto se encuentra localizado en forma iónica soluble en el espacio intratilacoidal y al iluminarse el cloroplasto pasa al estroma, donde activa enzimas como la rubisco, la fosfo-enolpiruvato carboxilasa y la glutamato sintasa. La asignación fotosintética del C y el N, depende en gran medida, de la concentración de Mg en el cloroplasto (Azcon Bieto y Talon, 2008). Cuando una planta es deficiente en Mg, disminuye el N proteico y aumenta el no proteico, por su efecto sobre las partículas ribosomales. Este hecho permite utilizar la medida del N no proteico soluble como índice de la deficiencia de Mg. Una sustancial proporción de este elemento está involucrada en la regulación del pH celular y el balance catión-anión. El Mg también interviene en el metabolismo energético de la planta al formar complejos con el ATP, estos permiten la fosforilación del ADP para transformarse en ATP. Si bien los síntomas de deficiencia de Mg varían de una especie a otra, existen algunas características generales que pueden citarse. A diferencia del Ca, los síntomas de deficiencia de Mg se concentran en las hojas inferiores debido a la alta movilidad de este nutriente dentro de las plantas, lo que determina una activa migración ante situaciones de deficiencia. Se producen clorosis internervales a causa de la menor fotosíntesis y acumulación de carbohidratos, ya que las células del mesófilo próximas a la nervadura conservan la clorofila por más tiempo. Finalmente, puede producirse necrosis en los casos más severos, empezando por las hojas maduras y avanzando hacia las más nuevas, a causa de su retranslocación vía floema. Las hojas se tornan rígidas y quebradizas, y suelen caer prematuramente. En el caso de los cereales, la base de las hojas muestra pequeñas manchas verde oscuro que se destacan sobre el resto del limbo, verde pálido amarillento. Finalmente se necrosan las puntas de las hojas. Los órganos de almacenamiento, tales como tubérculos o granos de cereales, pueden acumular menores cantidades de carbohidratos.
DIAGNÓSTICO DE LA FERTILIDAD CÁLCICA Y MAGNÉSICA
El diagnostico del nivel de Ca y Mg de los suelos ha estado tradicionalmente relacionado a determinaciones de pH y necesidades de encalado, ya que bajos niveles de pH están asociados con probables deficiencias de estos cationes. Pese a ello se han desarrollado metodologías con el objetivo de evaluar específicamente el contenido de Ca y Mg en los suelos en situaciones donde la acidez no es el problema principal. Una de las medidas más difundidas es la determinación de las fracciones intercambiables. En algunos casos estas evaluaciones de valores absolutos se enmarcan, para un diagnóstico más ajustado, en la saturación básica del suelo ((S=ΣCa, Mg, K, Na intercambiables/Capacidad de intercambio catiónico (CIC))*100), considerándose valores apropiados entre el 60-85%.
Además de la determinación de los contenidos absolutos de las formas intercambiables de Ca+2 y Mg+2 en el suelo, se han propuesto determinaciones de las cantidades relativas de estos cationes. En este sentido, el índice más difundido es el porcentaje de cada catión con respecto a la saturación básica del suelo (suma de bases intercambiables), concepto desarrollado originalmente por Bear y Toth (1948) y luego suscripto por numerosos autores, entre ellos, Zalewska (2003; 2005). De esta manera se propuso el concepto de una “relación ideal” entre algunos de los cationes que se encuentran adsorbidos en el complejo coloidal del suelo. Esta relación sugerida originalmente fue de 65% de Ca, 10% Mg, 5% de K y 20% de hidrogeno (H). Dicho concepto fue desarrollado luego de 8 años de trabajo en alfalfa en suelos de Nueva Jersey, EEUU. Si bien esta idea de una relación ideal entre cationes, ha sufrido severas críticas por parte de muchos investigadores desde su aparición, actualmente se la considera como parcialmente válida y existen ciertos resultados en la bibliografía donde se ha señalado su utilidad para diagnosticar deficiencia de algunos cationes para la nutrición vegetal. Se aceptan, en términos generales, saturaciones de cada uno de los nutrientes básicos respecto a la suma total de bases del orden de 65-85% de Ca, 6-12% de Mg y 2-5% de K.
Debe advertirse, sin embargo, que la evaluación de la saturación básica en su conjunto, como la de Ca, Mg o K en particular, empleando el método del acetato de amonio 1N pH 7, ampliamente difundido en el mundo y en Argentina, puede conducir a errores en el diagnóstico. La regulación a pH 7 en un suelo ácido, provoca un aumento artificial de la CIC, a través del aumento de las cargas variables de los coloides del suelo, resultando en porcentajes de saturación de estas bases bajos pero irreales. Es por este motivo que en suelos ácidos o tratados con correctores básicos deben utilizarse para la evaluación de la CIC, técnicas analíticas sin bufferación, poco difundidas en Argentina. Millán et al. (2010) evaluaron este efecto para suelos del ámbito pampeano, corroborando el hecho. Bajo este principio se propone utilizar en lugar de la CIC, la denominada capacidad de intercambio catiónico efectiva (CICE) determinada con cloruro de potasio (KCl 1 N), siendo:
CICE = Σ Ca, Mg, K, Na, Al Saturación de bases (%) = (Σ Ca, Mg, K, Na) *100/CICE
Zalewska (2008) informó que para girasol, la saturación óptima seria de 60% de Ca, 8,4 % de Mg y 4,2% de K. Saturaciones potásicas por debajo de 3% y por encima de 8% resultarían en considerables reducciones de rendimiento. La autora establece que la relación de saturación de Mg:K debe ser del orden de 2:1 para maximizar el rendimiento de este y otros cultivos (Zalewska 2003, 2005). Cabe destacar, sin embargo, que estos valores pueden cambiar considerablemente con la naturaleza coloidal en distintos suelos. Por ejemplo, Kamprath (1984) concluyó a través de un número de estudios, que saturaciones cálcicas de 20-30%, con 1 cmolc kg-1 de Ca intercambiable en suelos altamente meteorizados, dominados por caolinita y óxidos, fueron suficientes para la nutrición de la mayoría de las especies. Esto demuestra que las cifras citadas, son sólo orientativas, y en principio, no válidas para suelos muy evolucionados de ambientes subtropicales/tropicales. Otro aspecto fundamental a la hora de establecer estos umbrales, es el material genético de las especies cultivadas. Existen especies naturalmente resistentes a la toxicidad de aluminio (Al) y capaces de desarrollar con bajos suministros de bases, a la vez que en la actualidad se encuentran cultivares de varias especies seleccionados para estas condiciones de deficiencia.
Es por ambos motivos, características de los suelos y de las especies vegetales, que la literatura internacional es controvertida en el empleo de la saturación de las diferentes bases como elemento de diagnóstico. Varios autores, entre ellos Oliveira y Parra (2003), demostraron que grandes variaciones en la saturación de estos cationes tuvieron poca influencia sobre el rendimiento de especies cultivadas. De la misma manera, otros autores como Oliveira (1993), desestimaron el empleo de la relación Ca/Mg con este fin. Sin embargo varias investigaciones, entre ellas las de Muñoz Hernández y Silveira (1998), Büll et al. (1998), Anjos Reis et al. (1999), Borie et al. (1999), Demanet et al. (1999) y Loide (2004), por el contrario, verificaron la importancia de la saturación particular de estos cationes y sus relaciones, en el desarrollo de otras especies. Estos resultados permitirían concluir que el diagnóstico de suficiencia/deficiencia de los nutrientes básicos, debe ser calibrado para cada ambiente y cultivo a desarrollar, no pudiendo hacerse generalizaciones en este sentido, si bien los datos bibliográficos pueden servir de orientación para situaciones de cultivo/suelo comparables.
La saturación de cada uno de estos cationes en el complejo de intercambio, redunda en relaciones particulares entre los elementos básicos. Si bien no existen calibraciones regionales en el país y considerando que es común encontrar variación de los umbrales según otras condiciones edafo-climático-culturales, pueden, sólo a título de ejemplo, citarse algunos criterios de diagnóstico elaborados partir de una amplia revisión bibliográfica (Tabla 2).
Tabla 2. Umbrales críticos orientativos de relaciones entre cationes intercambiables.

Un valor superior a estos umbrales indicaría deficiencias relativas de los elementos del denominador. Por ejemplo, altos niveles de K a causa de un elevado contenido de micas e illita en la fracción mineral en el suelo, provocarían deficiencias inducidas de Ca y particularmente Mg. Esta situación está presente en muchas áreas de la Región Pampeana. Otros factores como baja temperatura, baja disponibilidad de P y condiciones de saturación hídrica, son predisponentes a estas deficiencias. De manera similar, este fenómeno puede producirse debido a altas dosis de fertilización potásica, las que suelen conducir a deficiencias relativas de Ca y Mg, aún en situaciones de adecuados contenidos de estos elementos en el pool intercambiable. Este hecho ha sido registrado en tabaco, caña de azúcar, papa y cebada. Darwich (2006) informó que la relación Ca/Mg no debe ser superior a 7/1.
La relación K/Mg es utilizada para decidir la fertilización magnésica, a la vez que identificar situaciones de hipomagnesemia o tetania de los rumiantes (Moseley y Baker, 1991). En general con valores de K/Mg superiores a 0,8 – 1,6/1 (en peso) en el suelo, es esperable esta alteración nutricional en animales que se alimentan mediante pasturas que crecen en estas condiciones. Concentraciones de Mg en forrajes menores a 2 g kg-1 y relaciones K/Ca+Mg mayores a 2,2, son factores predisponentes al problema. Según Darwich (2006) la relación K/Mg óptima para hortalizas, expresada en cmolc kg-1, se encuentra entre 1-1,5. En algunos suelos del SE bonaerense, el alto nivel de K intercambiable interfiere con la absorción de Mg (Darwich, 2006). De igual manera fue citada la deficiencia relativa de Mg a causa de elevados tenores de Ca para otros ámbitos de la Región Pampeana (Culot, 1967).
El problema principal que presenta este tipo de índices relativos es que su empleo puede derivar en conclusiones erróneas respecto a la suficiencia de ambos nutrientes. Esto ocurre porque una misma relación puede significar deficiencia o suficiencia de ambos nutrientes. Por ejemplo, si se consideran dos suelos, uno con 100 mg kg-1 de Ca+2 y 20 mg kg-1 de Mg+2 y otro con 300 mg kg-1 de Ca+2 y 60 mg kg-1 de Mg+2, ambos presentan la misma relación Ca/Mg. Sin embargo, el primer suelo seguramente será deficiente en ambos cationes mientas que el segundo presentará niveles adecuados de Ca y Mg para el crecimiento de la mayoría de las plantas. Es por esta razón que estas relaciones son evaluaciones complementarias a las de los valores absolutos para un correcto diagnóstico.
En cultivos intensivos y extensivos perennes, es común que el análisis del tejido vegetal sea una herramienta valiosa para el diagnóstico de Ca y Mg, así como de otros elementos. Esto se debe a que la respuesta de un cultivo de estas características no sólo está relacionada con la situación actual de la disponibilidad del nutriente en el suelo, sino también con su historia de crecimiento, que por ejemplo le confiere una cierta estructura radical y por ende capacidad de explorar suelo y captar nutrientes, estado sanitario, vigor, entre otras cosas.
En cultivos intensivos y extensivos perennes, es común que el análisis del tejido vegetal sea una herramienta valiosa para el diagnóstico de Ca y Mg, así como de otros elementos. Esto se debe a que la respuesta de un cultivo de estas características no sólo está relacionada con la situación actual de la disponibilidad del nutriente en el suelo, sino también con su historia de crecimiento, que por ejemplo le confiere una cierta estructura radical y por ende capacidad de explorar suelo y captar nutrientes, estado sanitario, vigor, entre otras cosas.
FERTILIZACIÓN DE CULTIVOS CON Ca Y Mg
1. Intensivos
La fertilización con Ca y Mg se hace regularmente en los cultivos bajo cubierta. La aplicación de estos nutrientes puede realizarse de varias formas (foliar, vía suelo, mediante el riego). También se los aplica como enmiendas, ya sea bajo la forma de calcita, dolomita o yeso, este último en suelos con altos niveles de Na. Existen fertilizantes que se aplican al suelo como lignosulfonato y quelato de Ca. Además, en fertirriego de especies ornamentales u hortícolas se suele usar como (NO3)2Ca en cantidades variables según cultivo y etapa fenológica. El Ca y el Mg también pueden aplicarse como quelatos en forma foliar. La absorción foliar del Ca por parte de las hojas es relativamente lenta, el 50% del Ca agregado puede demorar de 1 a 2 días (Romheld y El-Fouly, 2001). Por el contrario, la absorción foliar de Mg es muy rápida, generalmente las plantas pueden absorber el 50% del Mg aplicado entre de 2 a 5 h después de la aplicación. Existen diferentes productos para este tipo de fertilización. En general, el Ca se aplica en concentraciones de 200 a 300 g 100 l-1. En algunos programas se utiliza el (NO3)2Ca foliar complementando el que se aplica por fertirriego. Las concentraciones más comunes son: 300 a 450 g 100 l-1 de agua en la etapa reproductiva (Balcaza, comunicación personal). En cuanto al Mg, las aplicaciones pueden hacerse antes de la preparación del suelo, por ejemplo con SO4Mg.7H2O, en caso de situaciones de deficiencia, sin embargo, la fertirrigación es la práctica más difundida. Si bien estas dosis sugeridas son de uso bastante generalizado, es conveniente hacer un seguimiento de la solución del suelo a lo largo del ciclo del cultivo y evaluar en ella si las relaciones catiónicas se asemejan o no a las consideradas normales. Piaggio y Costa (1996) sugieren para la fertilización en estadios iniciales de tomate y pimiento una relación N:P:K:Mg:Ca:S de 1:0,4:1,5:0,1:0,5:0,1; mientras que cuando inicia la cosecha la relación aconsejada es 1:0:2,9:0,11:0,6:0,2. Silva y Larraín (1997) aconsejan 5 aplicaciones foliares de 1,5 kg ha-1 de Ca cada una, ya sea como cloruro, nitrato o fosfato, desde el estadío de frutos de 2,5 cm hasta 15 días antes de la cosecha, para reducir el efecto de bitter pit en manzano. Sin embargo, esta práctica debe acompañarse de otras condiciones de manejo referidas a niveles y momento de fertilización con otros nutrientes, podas y tratamientos poscosecha. Widmann (2002) comprobó que la aplicación de una fertilización mediante un complejo conteniendo 12% N, 12% P, 17% K y 2% Mg, a razón de 712 kg ha-1, produjo un incremento de la producción del 22% en naranjos en Corrientes. Vigil (2002) señala la importancia de lograr ciertas relaciones K/Mg en pecíolos y hojas de vides mendocinas vía fertilización, ya que las mismas afectan el desarrollo vegetativo, las características físico-químicas de las bayas, así como las características del mosto y el vino resultante. Se señala que la relación K/Mg foliar óptima en floración es 2,44. En los valles regados por los ríos Mendoza, Tunuyán, Diamante, Atuel y Malargüe en Mendoza, se registran algunos cultivos, como por ejemplo ciertos híbridos de tomate para mercado, en los cuales se fertiliza abundantemente con K. Esto suele provocar deficiencias inducidas de Mg que se tratan con aplicaciones de SO4Mg foliar. Otro problema que se presenta en la región es la podredumbre apical causada por la deficiencia de Ca en el extremo de los frutos. Este problema es motivado en la región, principalmente, por condiciones atmosféricas muy extremas, alta temperatura, muy baja humedad y fuerte viento (Zonda). Fertilizaciones con dosis muy elevadas de N, pueden incrementar la incidencia de este disturbio fisiológico (Lipinsky, comunicación personal).
2. Extensivos
La fertilización cálcico/magnésica en cultivos extensivos está menos desarrollada que en los cultivos intensivos. En general el inadecuado suministro de estos elementos está asociado a la acidificación del suelo, problemática que se trata mediante el encalado. Esta práctica utiliza productos naturales como la caliza (CaCO3) y la dolomita (MgCO3/CaCO3), entre los más difundidos, para la corrección de la acidez, incorporando Ca y Mg por esta vía. En ámbitos de reducida acidez, estos productos pueden utilizarse en bajas dosis, transformando la enmienda cuyo objetivo es corregir la acidez, en una fertilización, con el propósito de aportar Ca y Mg. Sin embargo existen fertilizantes de aplicación al suelo y foliares que contienen estos nutrientes.
A nivel nacional existen algunas experiencias donde se evaluó la respuesta de varios cultivos a fertilizaciones con Ca y Mg. Gambaudo et al. (2007) utilizaron 3 fertilizantes preparados a partir de compuestos minerales naturales, con aproximadamente 21-24% de Ca, y 8-9 % de Mg, además de S, Zn y Mn. Estos productos fueron aplicados en un cultivo de soja en 3 situaciones de la zona centro de Santa Fe, con dosis de 100-120 kg ha-1, obteniéndose incrementos de rendimiento de hasta 1000 kg ha-1. Martínez y Cordone (2008) evaluaron la respuesta al agregado de P, S y Mg del cultivo de soja en las Series Peyrano y Casilda del sur de Santa Fe. En esta experiencia, la fertilización magnésica se realizó con kierserita a una dosis de 11 kg ha-1 de Mg, y se observaron incrementos promedio de aproximadamente 150 kg de grano, por sobre el tratamiento con agregado de P y S. Vivas y Fontanetto (2003) verificaron en el centro de la Pcia. de Santa Fe, Dto. de San Justo, incrementos de rendimiento de soja del orden de 300 kg ha-1, con el agregado de 100 kg ha-1 de calcita micronizada y aperdigonada (Ca= 37%). Dosis superiores, 200-300 kg ha-1 del mismo producto, no provocaron incrementos de rendimiento adicionales. Melgar et al. (1999) observaron un incremento de 35% en el rendimiento de alfalfa en las localidades bonaerenses de 25 de Mayo y Pergamino, mediante el agregado de 30, 20 y 20 kg ha-1 de K, S y Mg (como MgO), respectivamente. Los dos suelos poseían relaciones 1,8 y 2,2 K/Mg, lo que indicaría posibilidad de respuesta a Mg, aspecto que se condijo con reducidos contenidos foliares de este elemento. El tratamiento mencionado superó en respuesta a las aplicaciones aisladas de estos elementos. Vivas et al. (2001) utilizaron un fertilizante granulado con 51% de CaCO3 y 37% de MgCO3, aplicado en dosis de hasta 600 kg ha-1 en maíz en suelos del centro de Santa Fe de pH 5,4 y 5,9 y bajos contenidos de Ca. Los resultados mostraron incrementos del rendimiento cercanos a los 1000 kg ha-1, con dosis de entre 400-600 kg ha-1, aproximadamente.
A nivel nacional existen algunas experiencias donde se evaluó la respuesta de varios cultivos a fertilizaciones con Ca y Mg. Gambaudo et al. (2007) utilizaron 3 fertilizantes preparados a partir de compuestos minerales naturales, con aproximadamente 21-24% de Ca, y 8-9 % de Mg, además de S, Zn y Mn. Estos productos fueron aplicados en un cultivo de soja en 3 situaciones de la zona centro de Santa Fe, con dosis de 100-120 kg ha-1, obteniéndose incrementos de rendimiento de hasta 1000 kg ha-1. Martínez y Cordone (2008) evaluaron la respuesta al agregado de P, S y Mg del cultivo de soja en las Series Peyrano y Casilda del sur de Santa Fe. En esta experiencia, la fertilización magnésica se realizó con kierserita a una dosis de 11 kg ha-1 de Mg, y se observaron incrementos promedio de aproximadamente 150 kg de grano, por sobre el tratamiento con agregado de P y S. Vivas y Fontanetto (2003) verificaron en el centro de la Pcia. de Santa Fe, Dto. de San Justo, incrementos de rendimiento de soja del orden de 300 kg ha-1, con el agregado de 100 kg ha-1 de calcita micronizada y aperdigonada (Ca= 37%). Dosis superiores, 200-300 kg ha-1 del mismo producto, no provocaron incrementos de rendimiento adicionales. Melgar et al. (1999) observaron un incremento de 35% en el rendimiento de alfalfa en las localidades bonaerenses de 25 de Mayo y Pergamino, mediante el agregado de 30, 20 y 20 kg ha-1 de K, S y Mg (como MgO), respectivamente. Los dos suelos poseían relaciones 1,8 y 2,2 K/Mg, lo que indicaría posibilidad de respuesta a Mg, aspecto que se condijo con reducidos contenidos foliares de este elemento. El tratamiento mencionado superó en respuesta a las aplicaciones aisladas de estos elementos. Vivas et al. (2001) utilizaron un fertilizante granulado con 51% de CaCO3 y 37% de MgCO3, aplicado en dosis de hasta 600 kg ha-1 en maíz en suelos del centro de Santa Fe de pH 5,4 y 5,9 y bajos contenidos de Ca. Los resultados mostraron incrementos del rendimiento cercanos a los 1000 kg ha-1, con dosis de entre 400-600 kg ha-1, aproximadamente.
La experimentación nacional en cereales es muy reducida. González et al. (2001) probaron el agregado de 100 kg ha-1 de un granulado calcáreo dolomítico con 22% de Ca y 13% de Mg, y 50 kg ha-1 un granulado de yeso con 22% de Ca y 18% de S, sobre un cultivo de trigo en San Nicolás, Pcia. Buenos Aires. Los productos fueron aplicados a la siembra y en línea, simultáneamente con una fertilización fosfórica (100 kg ha-1 de fosfato diamónico) y nitrogenada con 50 kg ha-1 de urea. Las enmiendas produjeron ligeros incrementos del rendimiento.
ACIDEZ DEL SUELO Y NECESIDAD DE ENCALADO
1. Principales fuentes de acidez
La acidez edáfica puede afectar el crecimiento de las plantas en forma directa, pero también indirecta, incidiendo negativamente en la disponibilidad de nutrientes, los niveles de elementos fitotóxicos, la actividad microbiana y hasta en las condiciones físicas de los suelos. Este problema es considerado como uno de las principales limitantes para la producción agropecuaria a nivel mundial. Aproximadamente 25-30% de los suelos del mundo están de alguna manera afectados por problemas de acidez y muchos de ellos se encuentran en las regiones más productivas (Havlin et al., 2005).
En regiones tropicales y subtropicales la problemática se origina en procesos genéticos naturales que provocan la pérdida de los elementos básicos contenidos en los materiales originales. Esto se debió, en la mayor parte de los casos, a materiales originales alterables de carácter ígneo básico, como por ejemplo el basalto en el NO argentino, y un clima agresivo de alta temperatura y pluviosidad. En esas condiciones, dichos materiales se meteorizaron intensamente y las bases, además de gran parte del Si, fueron lixiviadas. En estos ambientes sólo pueden desarrollarse especies vegetales adaptadas por su bajo requerimiento en estos elementos y tolerancia a efectos de toxicidad causados principalmente por el Al, y en situaciones extremas por el Fe, Mn y hasta el H, que insaturan el complejo de cambio.
En regiones templadas el proceso de acidificación se genera fundamentalmente por razones antrópicas, como se ha comentado precedentemente. Una de las causas de este proceso es la exportación de bases a través de la producción agropecuaria durante largos periodos de tiempo en regiones donde no ha existido historia de reposición de las mismas, mediante fertilización o aplicación de enmiendas básicas. A título de ejemplo se ilustra en la Figura 1 la exportación de Ca, Mg y K causada por la producción extensiva en la provincia de Santa Fe, durante 40 años comprendidos entre 1970 y 2010 (García y Vazquez, 2011).
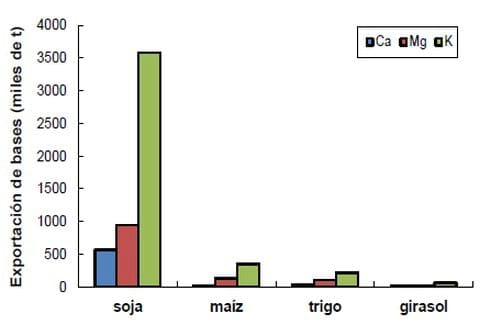 Figura 1. Exportación de bases de los suelos de la provincia de Santa Fe según cultivo para el período 1970-2010 (Extraído de García y Vázquez, 2011).
Figura 1. Exportación de bases de los suelos de la provincia de Santa Fe según cultivo para el período 1970-2010 (Extraído de García y Vázquez, 2011).
Otra de las causas de la acidificación es el aumento de la aplicación de fertilizantes de alto índice de acidez, fundamentalmente los nitrogenados amoniacales o con grupo amino, como la urea.
Por cada mol de sulfato de amonio se producen 4 moles de H+ y en el caso de la urea o del nitrato de amonio se generan 2 moles de protones, por lo que el primero de ellos debe considerarse más perjudicial. Estos son cálculos teóricos, ya que se demostró que en determinadas situaciones experimentales, la acidez generada por el sulfato de amonio era del 75% del valor teórico, mientras que la de urea o nitrato de amonio del 50%. Este aspecto magnifica la acidificación y posterior posibilidad de lixiviación de las bases causada por el sulfato de amonio.
Un trabajo realizado por Esterlich et al. (2012) con incubaciones de 2 suelos con 2 dosis de sulfato de amonio y urea (100 y 200 kg ha-1 año-1) simulando 10 años de la práctica, revelan la incidencia de estas fuentes nitrogenadas. En la Figura 2 se ilustran estos resultados para un Hapludol éntico frarenoso de la localidad de Bolívar, Pcia. De Buenos Aires.
Por cada mol de sulfato de amonio se producen 4 moles de H+ y en el caso de la urea o del nitrato de amonio se generan 2 moles de protones, por lo que el primero de ellos debe considerarse más perjudicial. Estos son cálculos teóricos, ya que se demostró que en determinadas situaciones experimentales, la acidez generada por el sulfato de amonio era del 75% del valor teórico, mientras que la de urea o nitrato de amonio del 50%. Este aspecto magnifica la acidificación y posterior posibilidad de lixiviación de las bases causada por el sulfato de amonio.
Un trabajo realizado por Esterlich et al. (2012) con incubaciones de 2 suelos con 2 dosis de sulfato de amonio y urea (100 y 200 kg ha-1 año-1) simulando 10 años de la práctica, revelan la incidencia de estas fuentes nitrogenadas. En la Figura 2 se ilustran estos resultados para un Hapludol éntico frarenoso de la localidad de Bolívar, Pcia. De Buenos Aires.
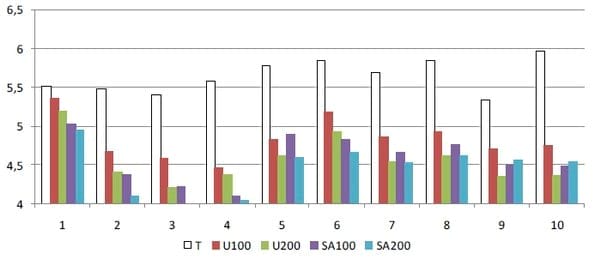
Figura 2. Evolución del pH actual en un suelo de tipo Hapludol éntico de la localidad de Bolívar simulando 10 años de agregado de 100 y 200 kg ha-1 año-1 de urea y sulfato de amonio (SA) (Extraído de Estelrich et al., 2012).
Sin embargo, cuando las incubaciones se realizan con desarrollo de cultivos, el efecto de los fertilizantes sobre la acidez del suelo sufre modificaciones.
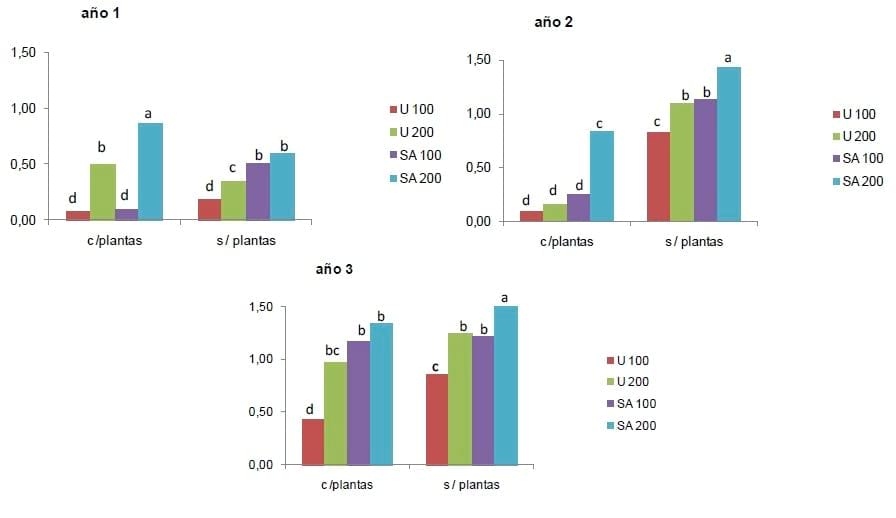
En la Figura 3 se ilustra la disminución del pH actual provocada por la fertilización con urea (U) y sulfato de amonio (SA) en dosis de 100 y 200 kg ha-1 año-1, durante 3 años sin cultivo y con el desarrollo de raygras (Lolium multiflorum L.) en un suelo de tipo Hapludol éntico de la misma localidad de Bolívar (Merani et al., 2014).
Figura 3. Disminución del pH actual en relación al testigo ante el agregado de 100 y 200 kg ha-1 de urea (U) y sulfato de amonio (SA) en un suelo sin y con cultivo de Lolium multiflorum (Extraído de Merani et al., 2014).
Esto puede deberse al balance de la absorción de nutrientes que forman aniones de ácidos fuertes como NO3 - ó SO4 2-, y bases como Ca2+, Mg2+ ó K+, además del mecanismo de absorción de nutrientes denominado bomba de protones.
Otros procesos que pueden derivar en la acidificación y lixiviación de bases en el suelo, son la hidrólisis de hierro y aluminio, la oxidación de compuestos de S y N nativos, la secreción de protones por las raíces, así como la respiración de microrganismos y las propias raíces. Estos procesos naturales de acidificación son de importancia secundaria en la región Pampeana Argentina en comparación con la magnitud de la remoción de bases y el uso de fertilizantes nitrogenados originados por la agricultura, particularmente de las últimas décadas.
Vázquez y Rotondaro (2005) evaluaron el pH de más de 4.000 muestras recibidas en el Laboratorio Suelo Fértil de la Asociación de Cooperativas Argentinas C.L. (ACA) correspondientes a las campañas 2004/5 y 2009/10 (Figura 4).
Otros procesos que pueden derivar en la acidificación y lixiviación de bases en el suelo, son la hidrólisis de hierro y aluminio, la oxidación de compuestos de S y N nativos, la secreción de protones por las raíces, así como la respiración de microrganismos y las propias raíces. Estos procesos naturales de acidificación son de importancia secundaria en la región Pampeana Argentina en comparación con la magnitud de la remoción de bases y el uso de fertilizantes nitrogenados originados por la agricultura, particularmente de las últimas décadas.
Vázquez y Rotondaro (2005) evaluaron el pH de más de 4.000 muestras recibidas en el Laboratorio Suelo Fértil de la Asociación de Cooperativas Argentinas C.L. (ACA) correspondientes a las campañas 2004/5 y 2009/10 (Figura 4).
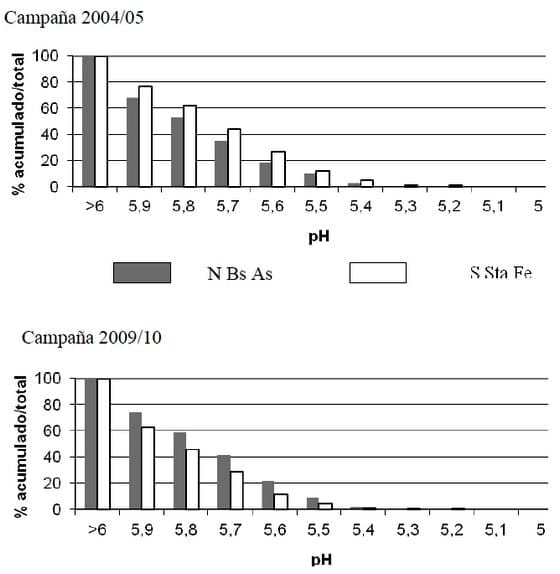
Figura 4. Porcentaje acumulado de valores menores de pH para 2 regiones de la Pampa Ondulada correspondientes a 2 campañas agrícolas (Extraído de Vázquez y Rotondaro, 2005).
Como puede apreciarse, alrededor del 70-75% de las muestras analizadas poseían pH inferior a 5,9, con ligeras diferencias para ambas campañas, situación crítica para cultivos como alfalfa y soja, demostrando la magnitud de la problemática en una de las zonas más productivas de Argentina. En un relevamiento hecho en forma conjunta FCAyF-UNLP con los laboratorios de suelos-agrupados en la Asociación de Laboratorios Agropecuarios Privados (ALAP) sobre más de 600 muestras en 3 subregiones de la Pcia. de Buenos Aires; 350 muestras de 2 subregiones de la Pcia de Córdoba y 290 muestras del S de Santa Fe, se encontraron los resultados de pH que se ilustran en la Figura 5.
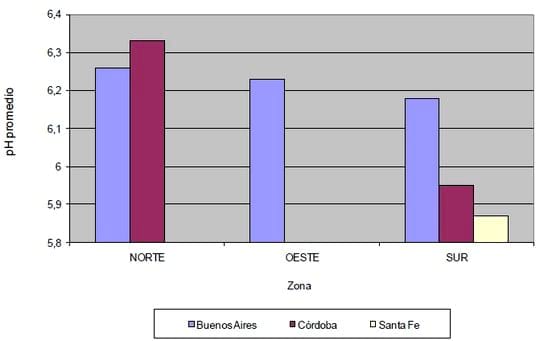
Figura 5. Valores promedio de pH actual (suelo:agua 1:2,5) en suelos de distintas subregiones de las Pcias. de Buenos Aires, Córdoba y Santa Fe (Datos no publicados de Vázquez et al., 2010).
Esta figura revela claramente que las zonas más afectadas son las subregiones S de las Pcias. de Córdoba y Santa Fe. Sin embargo el pH promedio de todas las subregiones evaluadas señala que la problemática de la acidificación en el corto plazo afectará, con alto grado de probabilidad, todas las áreas evaluadas. 2. Diagnóstico de necesidades de encalado La aplicación de enmiendas básicas al suelo y particularmente, el encalado, han sido las prácticas más comúnmente utilizadas para neutralizar la acidez edáfica. Debido a la importancia del proceso de acidificación sobre la capacidad productiva de los suelos, se ha destinado mucho esfuerzo en investigación tendiente a determinar el pH óptimo para el crecimiento de cada cultivo y desarrollar métodos para establecer requerimientos de encalado.
La literatura científica ha citado en muchas oportunidades rangos de pH óptimos para las diferentes especies. Este rango varía en valores y amplitud con las diferentes especies. En general es ampliamente aceptado que condiciones de neutralidad o ligera acidez son apropiadas para el crecimiento de la mayoría de las plantas. En la Tabla 3 se señalan pH óptimos y algunos rangos de tolerancia para especies vegetales de importancia económica.
La literatura científica ha citado en muchas oportunidades rangos de pH óptimos para las diferentes especies. Este rango varía en valores y amplitud con las diferentes especies. En general es ampliamente aceptado que condiciones de neutralidad o ligera acidez son apropiadas para el crecimiento de la mayoría de las plantas. En la Tabla 3 se señalan pH óptimos y algunos rangos de tolerancia para especies vegetales de importancia económica.
Tabla 3. pH óptimo y de tolerancia para especies vegetales cultivadas (Porta et al., 1999).
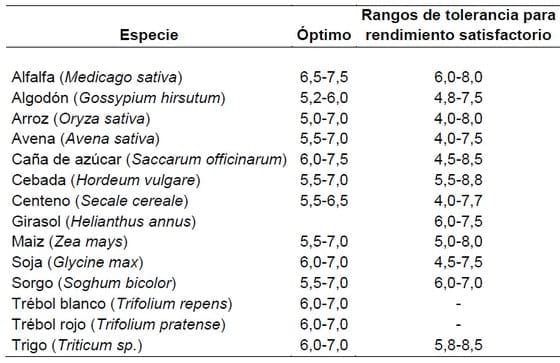
Cabe aclarar, que los valores de pH como los citados en la Tabla 3, son sólo orientativos, ya que el nivel crítico informado por diferentes autores es variable y posiblemente esté relacionado con otras propiedades edáficas como los niveles de Al y Mn, el contenido de materia orgánica y particularmente, el material genético utilizado. A título de ejemplo para el caso de la soja, Weisz et al. (2003) verificaron incrementos de rendimiento hasta valores de pH 6,0 en suelos de Carolina del Norte en EEUU. Pierce y Warncke (2000) informaron un valor crítico de 5,9 en suelos de Michigan por debajo del cual habría respuesta al encalado. Bell (1996) sugirió que dicho valor es 5,1 en suelos de Lousiana de alta meteorización, mientras que Caires et al. (1998) no obtuvieron respuesta al encalado aún con niveles de pH de 4,5 y 32% de saturación de bases en Brasil. Pagani et al. (2009) determinaron pH críticos para maíz y soja de aproximadamente 6.5 en Molisoles del estado de Iowa, EEUU. Estos antecedentes sugieren que el pH puede tener connotaciones distintas en diferentes tipos de suelos y sistemas productivos, mostrando lo inconveniente de la extrapolación de niveles críticos para cualquier especie. A pesar de las posibles limitaciones de este indicador, el pH del suelo es la principal herramienta utilizada mundialmente para diagnosticar problemas de acidez.
Existen diversos protocolos para la determinación del pH. Cuando se determina en suspensión suelo:agua (ó suelo CaCl2 0,01-0,02 M) de 1:1 a 1:2,5, es llamado “pH actual” en Argentina y en muchos otros países. Si bien el método más difundido es la determinación del pH del suelo en suspensiones suelo:agua, el uso de suspensiones suelo:CaCl2 ha sido recomendado como más estable y menos variable sobre todo en suelos con alto contenido de sales (Miller y Kissel, 2010), aunque no se han encontrado ventajas importantes de su utilización en suelos con bajos contenidos de sales (Pagani y Mallarino, 2011).
Esta determinación de pH actual, tanto en agua como en CaCl2, se realiza rutinariamente en los laboratorios. Dicho índice revela información acerca de la llamada “acidez activa” y cuantifica la actividad de H+ en la solución externa del suelo (no afectada por la carga de los coloides), pero no informa sobre la acidez de reserva o la capacidad reguladora (buffer) de un suelo. La determinación del pH en suspensiones suelo:KCl 1N, denominada pH potencial, permite cuantificar la concentración de H+ de la solución externa, y adicionalmente los H+ que se encuentran adsorbidos en el complejo de intercambio. Esta medida da idea de la reserva de H+. A título de ejemplo, dos suelos pueden tener igual pH actual, por ejemplo 6, y pH potencial 5,8 y 4,5, respectivamente. El segundo suelo tendrá una evolución más desfavorable a futuro y requerirá mayor cantidad de corrector para elevar el pH.
Existen diversos protocolos para la determinación del pH. Cuando se determina en suspensión suelo:agua (ó suelo CaCl2 0,01-0,02 M) de 1:1 a 1:2,5, es llamado “pH actual” en Argentina y en muchos otros países. Si bien el método más difundido es la determinación del pH del suelo en suspensiones suelo:agua, el uso de suspensiones suelo:CaCl2 ha sido recomendado como más estable y menos variable sobre todo en suelos con alto contenido de sales (Miller y Kissel, 2010), aunque no se han encontrado ventajas importantes de su utilización en suelos con bajos contenidos de sales (Pagani y Mallarino, 2011).
Esta determinación de pH actual, tanto en agua como en CaCl2, se realiza rutinariamente en los laboratorios. Dicho índice revela información acerca de la llamada “acidez activa” y cuantifica la actividad de H+ en la solución externa del suelo (no afectada por la carga de los coloides), pero no informa sobre la acidez de reserva o la capacidad reguladora (buffer) de un suelo. La determinación del pH en suspensiones suelo:KCl 1N, denominada pH potencial, permite cuantificar la concentración de H+ de la solución externa, y adicionalmente los H+ que se encuentran adsorbidos en el complejo de intercambio. Esta medida da idea de la reserva de H+. A título de ejemplo, dos suelos pueden tener igual pH actual, por ejemplo 6, y pH potencial 5,8 y 4,5, respectivamente. El segundo suelo tendrá una evolución más desfavorable a futuro y requerirá mayor cantidad de corrector para elevar el pH.
Un problema adicional se presenta para decidir reencalados, debido a que la residualidad de las enmiendas varía en los diferentes sistemas suelo-cultivo-clima. Aranzazu Sucunza et al. (2014) evaluaron 4 protocolos de determinación de pH: pH en agua y en KCl 1N, ambos con 2 diluciones, 1:1 y 1:2,5. La experiencia fue realizada con 2 suelos de la Región Pampeana en macetas que recibieron distintas dosis de dolomita y se incubaron por el término de 1 año. Los 4 protocolos utilizados estuvieron altamente asociados, particularmente los pH actuales en sus 2 diluciones entre sí, y los potenciales, igualmente, entre sí. El aumento de la dilución en las medidas produjo aumentos de pH potencial similar para ambos suelos y de pH actual mayor para el suelo Argiudol típico de textura franco-limoso, menor acidez y CIC. Las 4 medidas de pH fueron capaces de discriminar las dosis de encalado, aunque el pH actual 1:2,5 fue el que presentó las mayores diferencias en este sentido, señalándolo como más apropiado para este tipo de seguimiento.
El pH actual es generalmente utilizado para decir si un suelo necesita o no corrección mediante la aplicación de enmiendas básicas, pero no para determinar los requerimientos de encalado, es decir la dosis de enmienda necesaria para elevar el pH del suelo a un valor dado. Por esta razón, se han desarrollado numerosos métodos analíticos tendientes a determinar la cantidad de enmienda necesaria para neutralizar la acidez edáfica. Estos incluyen incubaciones de suelo, titulaciones directas y soluciones buffers, entre otros.
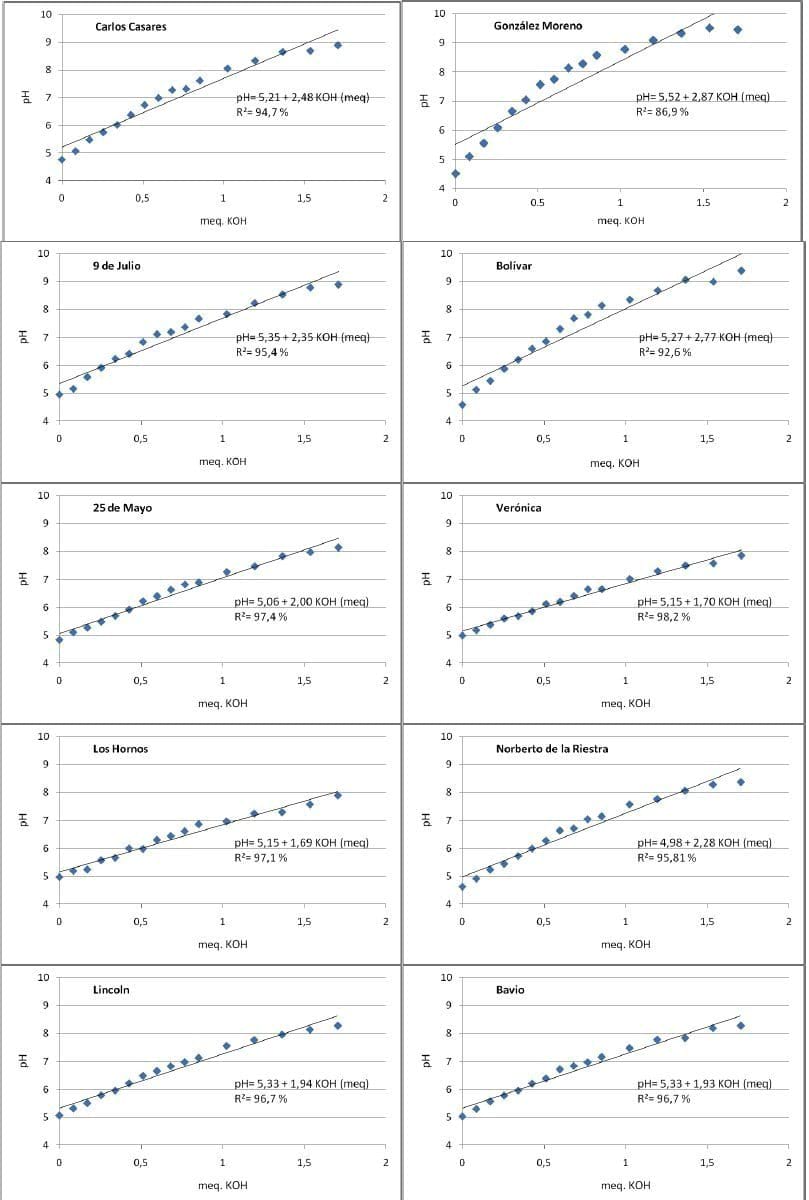
Las incubaciones de suelo consisten en la adición de diferentes dosis de CaCO3 u otra base en forma pura y finamente molida a un suelo. Luego el mismo se humedece y es incubado en cámara o invernáculo hasta alcanzar el equilibrio durante un periodo de semanas a meses, dependiendo de varios factores. Una vez que la base reacciona completamente, es decir se estabiliza el pH, se determina dicho valor de pH y se puede estimar el requerimiento. Bennardi et al. (2014), utilizando un método más expeditivo (Sadzawka et al., 2006) que incuba los suelos por 24 h con volúmenes crecientes de una solución de KOH (0,2M)/KCl(1M), obtuvo los resultados que se ilustran en la Figura 6 para 10 suelos de la Región Pampeana.
Estos mismos autores pudieron predecir la evolución del pH a través de la siguiente ecuación:
El pH actual es generalmente utilizado para decir si un suelo necesita o no corrección mediante la aplicación de enmiendas básicas, pero no para determinar los requerimientos de encalado, es decir la dosis de enmienda necesaria para elevar el pH del suelo a un valor dado. Por esta razón, se han desarrollado numerosos métodos analíticos tendientes a determinar la cantidad de enmienda necesaria para neutralizar la acidez edáfica. Estos incluyen incubaciones de suelo, titulaciones directas y soluciones buffers, entre otros.
Las incubaciones de suelo consisten en la adición de diferentes dosis de CaCO3 u otra base en forma pura y finamente molida a un suelo. Luego el mismo se humedece y es incubado en cámara o invernáculo hasta alcanzar el equilibrio durante un periodo de semanas a meses, dependiendo de varios factores. Una vez que la base reacciona completamente, es decir se estabiliza el pH, se determina dicho valor de pH y se puede estimar el requerimiento. Bennardi et al. (2014), utilizando un método más expeditivo (Sadzawka et al., 2006) que incuba los suelos por 24 h con volúmenes crecientes de una solución de KOH (0,2M)/KCl(1M), obtuvo los resultados que se ilustran en la Figura 6 para 10 suelos de la Región Pampeana.
Estos mismos autores pudieron predecir la evolución del pH a través de la siguiente ecuación:
b = 3,81 - 0,033 a (%) - 0,26 MO (%)
Siendo a: arcilla; MO: materia orgánica.
Ambas variables en el modelo fueron altamente significativas, y por tratarse de determinaciones de rutina en laboratorios de suelos, podrían ser utilizadas para la toma de decisión acerca de la dosis a emplear en la práctica del encalado.
Otra metodología utilizada para determinar acidez intercambiable y necesidades de encalado es la titulación simple (por única vez) con BaCl2-Trietanolamina a pH 8.2 (Bhumbla and McLean, 1965; Dietzel et al., 2009). Si bien este método es muy efectivo para cuantificar la acidez de reserva de un suelo, no es comúnmente empleado por laboratorios comerciales debido a su laboriosidad. Además, algunos resultados han sido desalentadores acerca de su utilidad para determinar requerimientos de encalado a campo (Pagani y Mallarino, 2012).
Debido a las dificultades prácticas y complejidad de los métodos descriptos, se han desarrollado métodos más sencillos y rápidos para determinar requerimientos de encalado en forma indirecta. Entre estos métodos se encuentran las soluciones reguladoras o buffers (mezcla de un acido débil con una base conjugada) que resisten cambios de pH pero que resultan en una disminución lineal del pH a medida que la acidez potencial del suelo reacciona con el buffer (Sims, 1996). Cuando el buffer se adiciona a una suspensión de suelo ácido y agua, se produce una disminución en el pH del sistema que es proporcional a la acidez de reserva de ese suelo, la cual está relacionada a la cantidad de corrector necesaria para neutralizar dicha acidez. Se requiere un estudio de calibración regional para determinar la relación entre los requerimientos de encalado (cantidad de material básico necesario para elevar el pH del suelo a un valor dado) y los valores de cierto buffer (Sims, 1996).
Los buffers originalmente propuestos para el medio-oeste americano y otras regiones de Norte America fueron el SMP (Shoemaker et al., 1961), buffer doble (Woodruff, 1948; Yuan, 1974); Adams-Evans (Adams y Evans, 1962) y Mehlich (Mehlich, 1976), entre otros. Sin embargo, estos métodos contienen reactivos tóxicos y peligrosos para el medioambiente como el p-paranitrofenol, K2CrO4 y BaCl2.2H2O. Por lo tanto, recientemente se han propuesto métodos que no contienen componentes peligrosos pero que brindan resultados similares o correlacionados a los buffers originalmente desarrollados (Pagani y Mallarino, 2012). Ejemplos de estos nuevos buffers son el Sikora (Sikora, 2006) y Mehlich modificado (Hoskins y Erich, 2008). Otro tipo de métodos de requerimientos de encalado que no requieren reactivos que comprometan el ambiente, son las titulaciones directas empleando adiciones simples de Ca(OH)2. Algunos estudios recientes en este sentido son los de Liu et al. (2005) y Kissel et al. (2007). Estos métodos se basan en el supuesto de que el incremento de pH de un suelo es lineal con la adición de una base en el rango entre 5 y 6.5 (Liu et al., 2005; Hoskins y Erich, 2008). Considerando esta asunción, un solo punto es suficiente para calcular los requerimientos de encalado.
Existen algunas experiencias nacionales referidas a la evaluación de métodos de requerimientos de encalado recomendados en distintas publicaciones, cuando se utilizan cálculos teóricos no calibrados para el sistema específico de producción (suelo-clima-material genético), utilizados en algunos laboratorios comerciales en el país. Vázquez et al. (2002) demostraron la variabilidad de resultados obtenidos por la aplicación de algunas de estas metodologías de diagnóstico (Tabla 4) y la ausencia de correlación entre los resultados de los diferentes métodos, así como entre el diagnóstico efectuado por ellos y la respuesta de la alfalfa al agregado de caliza o dolomita en ambientes templados.
Ambas variables en el modelo fueron altamente significativas, y por tratarse de determinaciones de rutina en laboratorios de suelos, podrían ser utilizadas para la toma de decisión acerca de la dosis a emplear en la práctica del encalado.
Otra metodología utilizada para determinar acidez intercambiable y necesidades de encalado es la titulación simple (por única vez) con BaCl2-Trietanolamina a pH 8.2 (Bhumbla and McLean, 1965; Dietzel et al., 2009). Si bien este método es muy efectivo para cuantificar la acidez de reserva de un suelo, no es comúnmente empleado por laboratorios comerciales debido a su laboriosidad. Además, algunos resultados han sido desalentadores acerca de su utilidad para determinar requerimientos de encalado a campo (Pagani y Mallarino, 2012).
Debido a las dificultades prácticas y complejidad de los métodos descriptos, se han desarrollado métodos más sencillos y rápidos para determinar requerimientos de encalado en forma indirecta. Entre estos métodos se encuentran las soluciones reguladoras o buffers (mezcla de un acido débil con una base conjugada) que resisten cambios de pH pero que resultan en una disminución lineal del pH a medida que la acidez potencial del suelo reacciona con el buffer (Sims, 1996). Cuando el buffer se adiciona a una suspensión de suelo ácido y agua, se produce una disminución en el pH del sistema que es proporcional a la acidez de reserva de ese suelo, la cual está relacionada a la cantidad de corrector necesaria para neutralizar dicha acidez. Se requiere un estudio de calibración regional para determinar la relación entre los requerimientos de encalado (cantidad de material básico necesario para elevar el pH del suelo a un valor dado) y los valores de cierto buffer (Sims, 1996).
Los buffers originalmente propuestos para el medio-oeste americano y otras regiones de Norte America fueron el SMP (Shoemaker et al., 1961), buffer doble (Woodruff, 1948; Yuan, 1974); Adams-Evans (Adams y Evans, 1962) y Mehlich (Mehlich, 1976), entre otros. Sin embargo, estos métodos contienen reactivos tóxicos y peligrosos para el medioambiente como el p-paranitrofenol, K2CrO4 y BaCl2.2H2O. Por lo tanto, recientemente se han propuesto métodos que no contienen componentes peligrosos pero que brindan resultados similares o correlacionados a los buffers originalmente desarrollados (Pagani y Mallarino, 2012). Ejemplos de estos nuevos buffers son el Sikora (Sikora, 2006) y Mehlich modificado (Hoskins y Erich, 2008). Otro tipo de métodos de requerimientos de encalado que no requieren reactivos que comprometan el ambiente, son las titulaciones directas empleando adiciones simples de Ca(OH)2. Algunos estudios recientes en este sentido son los de Liu et al. (2005) y Kissel et al. (2007). Estos métodos se basan en el supuesto de que el incremento de pH de un suelo es lineal con la adición de una base en el rango entre 5 y 6.5 (Liu et al., 2005; Hoskins y Erich, 2008). Considerando esta asunción, un solo punto es suficiente para calcular los requerimientos de encalado.
Existen algunas experiencias nacionales referidas a la evaluación de métodos de requerimientos de encalado recomendados en distintas publicaciones, cuando se utilizan cálculos teóricos no calibrados para el sistema específico de producción (suelo-clima-material genético), utilizados en algunos laboratorios comerciales en el país. Vázquez et al. (2002) demostraron la variabilidad de resultados obtenidos por la aplicación de algunas de estas metodologías de diagnóstico (Tabla 4) y la ausencia de correlación entre los resultados de los diferentes métodos, así como entre el diagnóstico efectuado por ellos y la respuesta de la alfalfa al agregado de caliza o dolomita en ambientes templados.
Figura 6. Curvas de titulación de 10 suelos de la Región Pampeana (extraído de Bennardi et al., 2014)
Cabe aclarar que la utilización del valor de pH del suelo, la capacidad buffer o su reacción ante el agregado de un buffer como herramientas de diagnóstico y recomendación de encalado, tiene particular importancia en suelos cuyo pH esta por debajo de 5,3-5,5, situación de solubilización del Al y por lo tanto, posibilidades de toxicidad de este elemento. Esto generalmente ocurre en suelos de áreas subtropicales-tropicales.
Cuando la situación de acidez es extrema, por ejemplo en Oxisoles y Ultisoles, y el porcentaje de saturación básica es muy bajo, problemática asociada a suelos de regiones tropicales y subtropicales, el objetivo puede ser reducir la acidez y elevar la saturación básica en su conjunto. En tales casos, puede emplearse un cálculo simple para estimar la cantidad de corrector (CaCO3) a utilizar:
NC = CIC (V2 – V1) / EQ
NC: Necesidad de corrector (CaCO3 (t ha-1))
CIC: Capacidad de intercambio catiónica (cmolc kg-1)
V2: Saturación básica deseada (%)
V1: Saturación básica real (%) EQ: Eficiencia química del corrector (%) (concepto que se abordará más adelante)
Cuando la situación de acidez es extrema, por ejemplo en Oxisoles y Ultisoles, y el porcentaje de saturación básica es muy bajo, problemática asociada a suelos de regiones tropicales y subtropicales, el objetivo puede ser reducir la acidez y elevar la saturación básica en su conjunto. En tales casos, puede emplearse un cálculo simple para estimar la cantidad de corrector (CaCO3) a utilizar:
NC = CIC (V2 – V1) / EQ
NC: Necesidad de corrector (CaCO3 (t ha-1))
CIC: Capacidad de intercambio catiónica (cmolc kg-1)
V2: Saturación básica deseada (%)
V1: Saturación básica real (%) EQ: Eficiencia química del corrector (%) (concepto que se abordará más adelante)
Tabla 4. Necesidad de encalado (CaCO3) según diferentes técnicas diagnóstico (Vázquez et al., 2002).
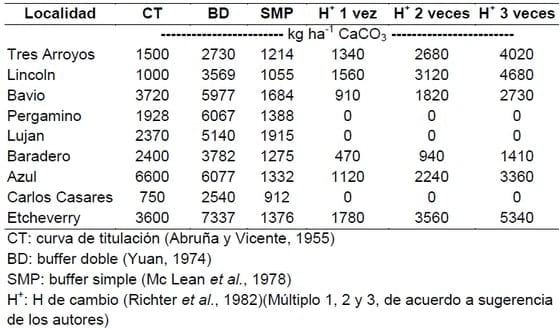
En caso de utilizar otro producto deberá corregirse el resultado según la Tabla 5. Algunos autores modifican el resultado obtenido por esta ecuación, a través de un factor del orden de 1,5, con la finalidad de considerar reacciones paralelas de los correctores en la neutralización del Al no intercambiable relacionado con la materia orgánica (Cochrane et al., 1980). En este tipo de suelos ácidos otro elemento de juicio es el porcentaje de Al intercambiable. Las diferentes especies toleran cantidades variables de insaturación con Al intercambiable. Por ejemplo, trigo y soja no toleran porcentajes de Al intercambiable > 10%, sorgo > al 20% y maíz al > 25% (Carver y Ownby, 1995; Kollmeier et al., 2000; Villagarcía et al., 2001).
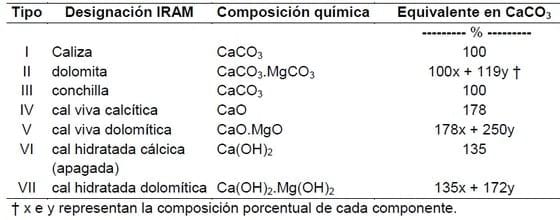
Tabla 5. Equivalentes en carbonato de calcio de los materiales calcáreos más utilizados para uso agropecuario (Norma IRAM 22451).
Numerosos estudios han demostrado extensa variabilidad espacial del pH del suelo y necesidades de encalado dentro de los lotes de producción. Pierce y Warncke (2000) sugieren la conveniencia de la aplicación de los productos encalantes mediante técnicas de agricultura de precisión (manejo de sitio específico a través del empleo de dosis variable) a los fines de evitar sub o sobreaplicaciones. En este sentido, Pagani y Mallarino (2012a) determinaron lotes contrastantes en cuanto a variabilidad espacial de pH del suelo, buffers y requerimientos de encalado en el estado de Iowa, EEUU. En la misma región, Bianchini y Mallarino (2002) señalaron que la aplicación de corrector en forma variable dentro del lote ayudaba a disminuir la variabilidad espacial del pH edáfico. Al igual que para otros nutrientes, la tecnología de aplicación variable de corrector, requiere de un muestreo de suelos intensivo, el cual puede ser en grillas regulares, en zonas o mediante el uso de instrumentos que colectan muestras de suelo y analizan su pH en tiempo real. Además, se requiere de aplicadores que, guiados por sistemas de geoposicionamiento global (GPS) y mapas de prescripción, puedan realizar aplicaciones efectuando cambios de dosis en tiempo real. Si este sistema se utiliza correctamente, puede derivar en ahorros en la cantidad de material calcáreo, mayores eficiencias de uso de la enmienda y, eventualmente, en aumentos en la producción de los cultivos.
3. Tipos de enmiendas calcáreas y tecnología del encalado
Tradicionalmente para la corrección de acidez se han usado productos correctores o enmiendas, tales como calcita, dolomita y cal viva o apagada, entre otros. Estos productos que contienen Ca y/o Mg en diferentes proporciones, han dado origen a la práctica denominada encalado. La aplicación de materiales básicos como CaCO3, CaO o Ca(OH)2, produce 2 efectos en el suelo, uno meramente nutricional, que es el suministro de Ca y/o Mg, y por otro, produce un incremento en el pH del suelo, neutralizando los H+ y disminuyendo la solubilidad del Al+3. Si bien el pH del suelo podría elevarse a través del agregado de otros compuestos, generalmente se emplean los cálcico/magnésicos con el objetivo de reponer estos elementos con funciones nutricionales para los cultivos, así como de estructurantes edáficos en suelos de regiones templadas, ya que mejoran la dinámica del aire y el agua del suelo.
Los valores de equivalentes de CaCO3 presentados en la Tabla 5 son considerados teóricos ya que algunos estudios como el de Alcarde y Rodella (1996) demostraron que la presencia de fosfatos, sulfatos o de cristales de Si en los productos correctores, podrían modificar esta equivalencia teórica.
Para agregar CaCO3 puede utilizarse caliza, la cual contiene alrededor de 40% de CaCO3, o dolomita, que posee alrededor de 21% de CaCO3 y 13% de MgCO3. Estos valores son variables por tratarse de productos de minería. De la misma manera puede utilizarse conchilla molida, que cuenta con un porcentaje de CaCO3 mayor al 90%. La cal viva (CaO) se obtiene por calcinación del CaCO3, es un producto cáustico y de alta higroscopicidad, aunque de gran velocidad de reacción y poder de neutralización. La cal apagada (Ca(OH)2) se obtiene hidratando la cal viva. Existen otros productos utilizados con este fin, tales como espumas azucareras, residuos calcáreos de la fabricación del papel, la cola de cal, un subproducto de la fabricación del cemento y residuos de la industria del acero, que contienen elevados porcentajes de silicatos de Ca y Mg, conocidos como Escorias Thomas, las que además se caracterizan por un cierto contenido de P, por lo que son usados como fertilizantes fosforados.
Las tasas de aplicación de los materiales para encalar van desde unos cientos de kg ha-1, hasta cifras del orden de las 4-6 t de producto ha-1 o superiores. Las cantidades requeridas varían de acuerdo al criterio del empleo de estos productos. En caso de suelos de pH muy bajo, donde el objetivo es reducir la acidez, la cantidad a aplicar depende justamente de la acidez actual y potencial del suelo, su poder buffer, así como del pH o porcentaje de saturación básica que se desean alcanzar. Mientras que en situaciones donde la acidez no es pronunciada, la cantidad y tipo de corrector a elegir, dependerán de la necesidad de Ca y/o Mg, analizados desde el punto de vista de la nutrición vegetal. En general las cantidades a que se arriba en este segundo caso son significativamente menores. Vázquez et al. (2002) demostraron que en suelos de la provincia de Buenos Aires, la alfalfa respondió en forma diferencial en algunos casos, al agregado de caliza y dolomita, demostrando la necesidad específica de alguna de las bases, mientras que en otros casos la respuesta a estos productos fue equivalente (Figura 7).
3. Tipos de enmiendas calcáreas y tecnología del encalado
Tradicionalmente para la corrección de acidez se han usado productos correctores o enmiendas, tales como calcita, dolomita y cal viva o apagada, entre otros. Estos productos que contienen Ca y/o Mg en diferentes proporciones, han dado origen a la práctica denominada encalado. La aplicación de materiales básicos como CaCO3, CaO o Ca(OH)2, produce 2 efectos en el suelo, uno meramente nutricional, que es el suministro de Ca y/o Mg, y por otro, produce un incremento en el pH del suelo, neutralizando los H+ y disminuyendo la solubilidad del Al+3. Si bien el pH del suelo podría elevarse a través del agregado de otros compuestos, generalmente se emplean los cálcico/magnésicos con el objetivo de reponer estos elementos con funciones nutricionales para los cultivos, así como de estructurantes edáficos en suelos de regiones templadas, ya que mejoran la dinámica del aire y el agua del suelo.
Los valores de equivalentes de CaCO3 presentados en la Tabla 5 son considerados teóricos ya que algunos estudios como el de Alcarde y Rodella (1996) demostraron que la presencia de fosfatos, sulfatos o de cristales de Si en los productos correctores, podrían modificar esta equivalencia teórica.
Para agregar CaCO3 puede utilizarse caliza, la cual contiene alrededor de 40% de CaCO3, o dolomita, que posee alrededor de 21% de CaCO3 y 13% de MgCO3. Estos valores son variables por tratarse de productos de minería. De la misma manera puede utilizarse conchilla molida, que cuenta con un porcentaje de CaCO3 mayor al 90%. La cal viva (CaO) se obtiene por calcinación del CaCO3, es un producto cáustico y de alta higroscopicidad, aunque de gran velocidad de reacción y poder de neutralización. La cal apagada (Ca(OH)2) se obtiene hidratando la cal viva. Existen otros productos utilizados con este fin, tales como espumas azucareras, residuos calcáreos de la fabricación del papel, la cola de cal, un subproducto de la fabricación del cemento y residuos de la industria del acero, que contienen elevados porcentajes de silicatos de Ca y Mg, conocidos como Escorias Thomas, las que además se caracterizan por un cierto contenido de P, por lo que son usados como fertilizantes fosforados.
Las tasas de aplicación de los materiales para encalar van desde unos cientos de kg ha-1, hasta cifras del orden de las 4-6 t de producto ha-1 o superiores. Las cantidades requeridas varían de acuerdo al criterio del empleo de estos productos. En caso de suelos de pH muy bajo, donde el objetivo es reducir la acidez, la cantidad a aplicar depende justamente de la acidez actual y potencial del suelo, su poder buffer, así como del pH o porcentaje de saturación básica que se desean alcanzar. Mientras que en situaciones donde la acidez no es pronunciada, la cantidad y tipo de corrector a elegir, dependerán de la necesidad de Ca y/o Mg, analizados desde el punto de vista de la nutrición vegetal. En general las cantidades a que se arriba en este segundo caso son significativamente menores. Vázquez et al. (2002) demostraron que en suelos de la provincia de Buenos Aires, la alfalfa respondió en forma diferencial en algunos casos, al agregado de caliza y dolomita, demostrando la necesidad específica de alguna de las bases, mientras que en otros casos la respuesta a estos productos fue equivalente (Figura 7).
Loide (2004), Järvan (2004) y Järvan y Põldma (2004) demostraron la incidencia del tipo de corrector sobre el rendimiento de diversas especies, a igualdad de dosis, explicando el fenómeno a través del pH alcanzado en cada caso y el balance catiónico de los mismos. En la Figura 8 puede apreciarse la modificación del pH producido en tres suelos de la Pcia. de Buenos Aires por el agregado de caliza y dolomita en diferentes dosis (Vázquez et al., 2002). Estos productos pueden aplicarse en cualquier época del año. En general se anticipan algunos meses a los cultivos de mayor sensibilidad, incorporándolos al suelo, para permitir su solubilización. Sin embargo, en planteos de siembra directa Ciotta et al. (2004) y Amaral et al. (2004) demostraron que la aplicación en superficie de caliza puede tener efecto hasta los 20 cm de profundidad. Farina et al. (2000), Caires et al. (2003) y Vázquez et al. (2008) comprobaron que la aplicación conjunta de caliza y yeso mejora la movilización profunda del Ca, en aplicaciones superficiales de los productos. Vázquez et al. (2010, 2012) comprobaron respuesta a campo de la práctica para los cultivos de alfalfa) y soja) en suelos de la Región Pampeana. En las Figuras 9 y 10 se ilustran los resultados de 2 de los ensayos realizados por los investigadores. En ambos casos resultaron más eficientes las dosis menores de encalado. En el apartado siguiente se expondrán algunas posibles razones.
La FCAyF/UNLP en forma conjunta con una empresa del sector de agroinsumos desarrolló 2 productos mixtos aperdigonados conteniendo sales solubles e insolubles de Ca y Mg. Este desarrollo pretende disminuir el problema de deriva en la aplicación y mejorar la disolución y migración en el perfil del corrector, particularmente con el objetivo de su empleo en siembra directa. Para su evaluación se realizó un ensayo en macetas con 11 suelos de diferentes texturas, en condiciones controladas con aplicación superficial y mezclada en la masa de suelo, comparando dolomita y ambos productos. En la experiencia se evaluó la materia seca desarrollada por trébol rojo (Trifolium pratense cultivar Red Land II) previamente inoculado y la lixiviación de Ca y Mg. En la Figura 11 se ilustra la respuesta vegetal a los tratamientos aplicados para 2 de los suelos con texturas contrastantes. En la Figura 12 se muestran las cantidades de bases lixiviadas a los 6 meses de la aplicación de los productos, tras la percolación del 150% de la capacidad de retención de agua de cada suelo.
La FCAyF/UNLP en forma conjunta con una empresa del sector de agroinsumos desarrolló 2 productos mixtos aperdigonados conteniendo sales solubles e insolubles de Ca y Mg. Este desarrollo pretende disminuir el problema de deriva en la aplicación y mejorar la disolución y migración en el perfil del corrector, particularmente con el objetivo de su empleo en siembra directa. Para su evaluación se realizó un ensayo en macetas con 11 suelos de diferentes texturas, en condiciones controladas con aplicación superficial y mezclada en la masa de suelo, comparando dolomita y ambos productos. En la experiencia se evaluó la materia seca desarrollada por trébol rojo (Trifolium pratense cultivar Red Land II) previamente inoculado y la lixiviación de Ca y Mg. En la Figura 11 se ilustra la respuesta vegetal a los tratamientos aplicados para 2 de los suelos con texturas contrastantes. En la Figura 12 se muestran las cantidades de bases lixiviadas a los 6 meses de la aplicación de los productos, tras la percolación del 150% de la capacidad de retención de agua de cada suelo.
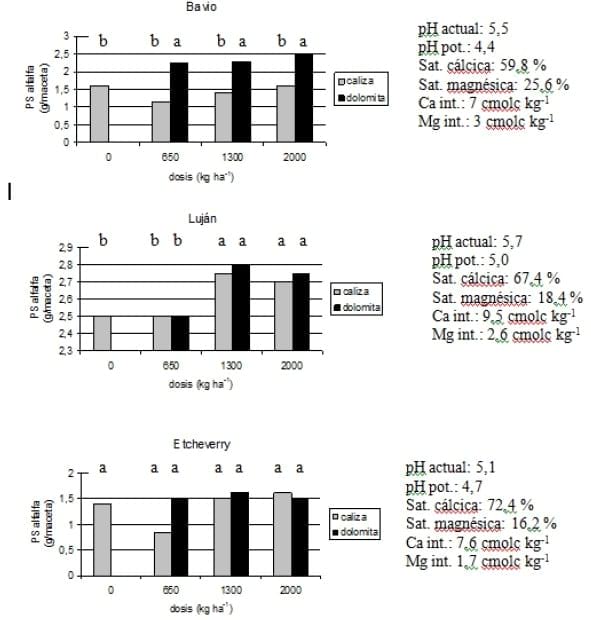
Figura 7. Respuesta de la alfalfa al agregado de caliza (CaCO3) y dolomita (CaCO3.MgCO3) en 3 suelos de la Pcia. de Buenos Aires (Extraído de Vázquez et al., 2002).
Como puede verse en ambas figuras, el empleo de enmiendas que combinan sales insolubles y solubles de bases fueron mayoritariamente más efectivas en el aumento de la materia seca de la especie analizada que una dolomita comercial pulverulenta, a igualdad de dosis, no pudiendo establecerse diferencias entre los 2 productos desarrollados. La aplicación superficial de Y1 en la dosis superior no redujo la producción de materia seca respecto de su aplicación con incorporación, mientras que este hecho ocurrió en varios suelos con la dolomita comercial. Esto sugiere que el producto desarrollado es más conveniente para planteos de siembra directa. Los productos desarrollados produjeron mayores lixiviaciones de Ca y Mg tanto en su aplicación mezclados en la masa de suelo como superficial, en relación a la dolomita, confirmando su eficacia para la movilización profunda de las bases, explicando la respuesta en materia seca. Los resultados obtenidos por los investigadores señalan la necesidad y posibilidad de desarrollo de enmiendas más apropiadas para aplicaciones superficiales como las necesarias en planteos de siembra directa.
Un tema a considerar es que en algunos casos de suelos encalados se ha demostrado respuesta a la aplicación de fertilizantes fosforados, aun a valores de P extractable no señalados como limitantes para los cultivos. Este hecho deriva de la inmovilización temporaria de P provocada por la precipitación con Ca/Mg contenidos en los correctores. La Figura 10 ilustra una situación de esta naturaleza en un suelo con 24 mg kg-1 de P extractable por método Bray-1.
Un tema a considerar es que en algunos casos de suelos encalados se ha demostrado respuesta a la aplicación de fertilizantes fosforados, aun a valores de P extractable no señalados como limitantes para los cultivos. Este hecho deriva de la inmovilización temporaria de P provocada por la precipitación con Ca/Mg contenidos en los correctores. La Figura 10 ilustra una situación de esta naturaleza en un suelo con 24 mg kg-1 de P extractable por método Bray-1.
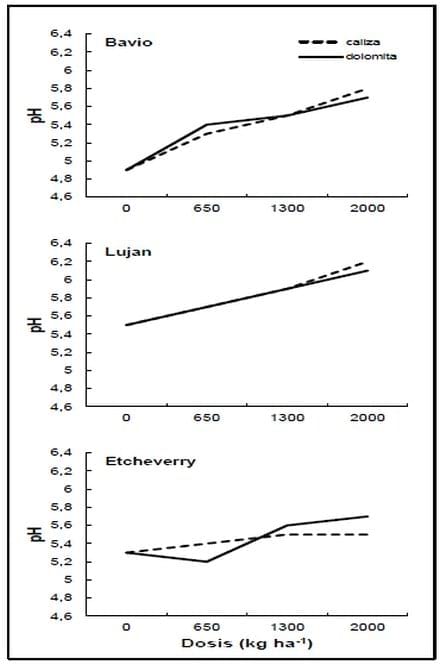
Figura 8. Evolución del pH ante el agregado de 3 dosis de caliza (CaCO3) y dolomita (CaCO3.Mg CO3) en 3 suelos de la Pcia. de Buenos Aires (Extraído de Vázquez et al., 2002).
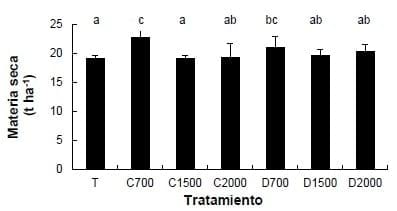
Figura 9. Efecto del tratamiento de encalado sobre la producción de materia seca de alfalfa en 10 cortes en un suelo Hapludol entico con pH 5,1 de la localidad de Laboulaye, Prov. de Córdoba. Letras distintas indican diferencias estadísticas significativas (p<0,05) entre tratamientos. Referencia: T: testigo; C: caliza; D: dolomita. Dosis: 700, 1500 y 2000 kg ha-1. (Extraído de Vázquez et al., 2010).
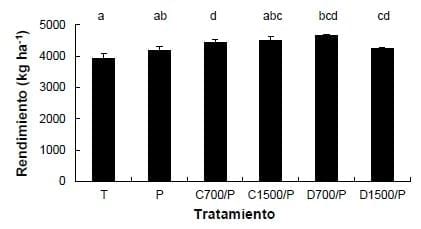
Figura 10. Efecto de los tratamientos de encalado sobre el rendimiento de soja en un suelo Argiudol thaptoárgico con pH 5,7 de Lincoln, Prov. de Buenos Aires. Letras distintas indican diferencias estadísticas significativas (p<0,05) entre tratamientos. Referencia: T: testigo; P (Fósforo): 100 kg ha-1 de superfosfato triple; C: caliza; D: dolomita. Dosis de corrector: 700 y 1500 kg ha-1. (Extraído de Vázquez et al., 2012).
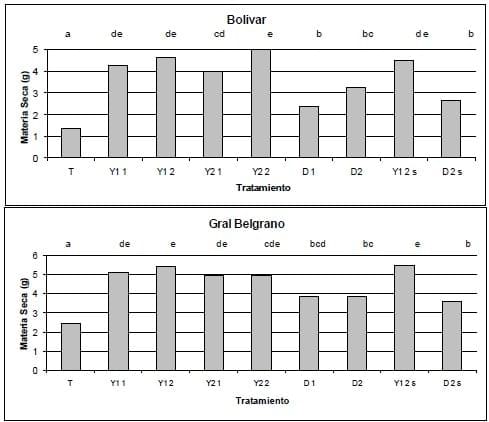
Referencia: Y1, Y2 (productos mixtos aperdigonados), D: dolomita; s: agregado superficial; dosis: T(testigo); 1 (equivalente a 1.500 kg ha-1), 2 (equivalente a 3.000 kg ha-1). Letras diferentes indican diferencias estadísticas significativas (p< 0,05).
Figura 11. Respuesta en materia seca de Trebol rojo al agregado de dolomita y correctores mixtos en un suelos de textura fr-A (Bolívar) y arcillosa (Belgrano) (Datos no publicados de Vázquez et al., 2014).
Figura 11. Respuesta en materia seca de Trebol rojo al agregado de dolomita y correctores mixtos en un suelos de textura fr-A (Bolívar) y arcillosa (Belgrano) (Datos no publicados de Vázquez et al., 2014).
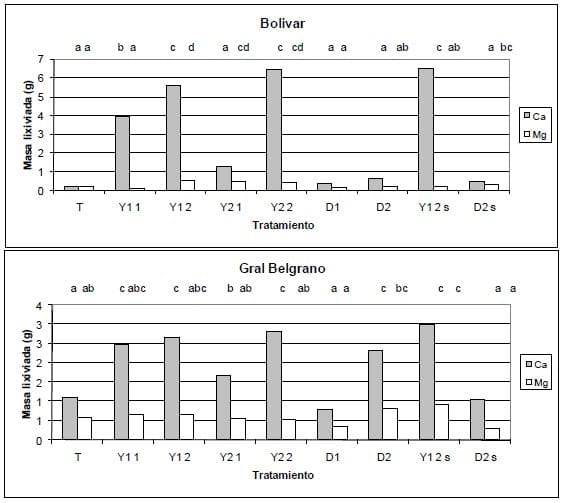 Referencia: Y1, Y2 (productos mixtos aperdigonados), D: dolomita; s: agregado superficial; dosis: T(testigo); 1 (equivalente a1.500 kg ha-1), 2 (equivalente a 3.000 kg ha-1)
Referencia: Y1, Y2 (productos mixtos aperdigonados), D: dolomita; s: agregado superficial; dosis: T(testigo); 1 (equivalente a1.500 kg ha-1), 2 (equivalente a 3.000 kg ha-1)
Figura 12. Contenido de Ca y Mg en los lixiviados 6 meses a posteriori de la aplicación de dolomita y 2 productos aperdigonados mixtos en 2 suelos de texturas contrastantes (Datos no publicados de Vázquez et al., 2014).
La periodicidad de la aplicación de los correctores va desde frecuencias anuales, en situaciones de elevada acidez y cultivos sensibles, a encalados cada 2-4 años, en situaciones menos limitantes. La periodicidad depende de su residualidad en cada sistema suelo-planta. Así alta temperatura y humedad, como acidez del suelo, favorecen la solubilidad de los correctores, y por lo tanto la residualidad de las enmiendas básicas se ve reducida en ambientes tropicales. En este tipo de suelos y en situaciones de texturas gruesas, el movimiento profundo de las bases es mayor y por lo tanto se reduce la residualidad. Los óxidos e hidróxidos de bases fuertes reaccionan más rápido que las sales de bases débiles, tales como los carbonatos, incidiendo de esa manera en la residualidad de la práctica. Cuanto mayor es el tamaño de partícula, menor la reacción inmediata y mayor el efecto a más largo plazo. A menor dosis, menor residualidad y a mayor exportación de bases por la producción y mayores dosis de fertilizantes de carácter ácido, a posteriori de la práctica, menor la residualidad del producto.
4. Algunos efectos secundarios del encalado
El aumento del pH del suelo puede acarrear algunos efectos secundarios, entre ellos la modificación de la estabilidad de los agregados edáficos. En suelos ácidos el incremento de pH disminuye las cargas variables positivas y con ellas podría disminuir la estabilidad estructural (Roth y Pavan, 1991). Albuquerque et al. (2003) demostraron que si bien ocurre un aumento de la dispersión de arcilla con la dosis de calcáreo en el caso de un suelo del planalto brasilero, el mayor aporte orgánico originado por el beneficio del encalado, compensa el proceso dispersivo, no alterándose en consecuencia la estabilidad estructural. Como puede verse, el fenómeno es multivariable y es necesario profundizar en estos procesos para diferentes ambientes edafo-climáticos. Otros autores, por el contrario, han puesto en evidencia una mejora en dicha propiedad, haciendo referencia a la formación de puentes cálcicos que favorecen la floculación de los coloides del suelo (Chan y Heenan, 1999). Las diferencias encontradas radican en las cargas dominantes de los coloides en cada tipo de suelo, las cuales están relacionadas con la mineralogía y acidez del mismo, por lo que no se puede hacer generalizaciones en este sentido.
Relacionado con la modificación de las propiedades físicas, Vázquez et al. (2009) encontraron que el agregado de caliza y dolomita modificó la resistencia a la penetración en forma variable según dosis/profundidad de evaluación en suelos del Pdo. de La Plata (Buenos Aires). Los autores destacaron que dosis bajas del orden de 1.000 kg ha-1 redujeron la resistencia respecto del testigo, afirmando su acción sobre la estructuración del suelo. Sin embargo, se advirtió que dosis más elevadas, 1.500 y 2.000 kg ha-1, por el contrario, aumentaban la resistencia respecto del testigo, argumentando que podría tratarse de recristalización de los carbonatos. Esta recristalización obturaría el espacio poroso en los suelos de textura fina y por ende con predominio de poros de tamaño pequeño. Estos resultados se asociaron con medidas biológicas (desarrollo de hongos y rendimiento de alfalfa), por lo que en suelos de texturas finas podrían ser desaconsejadas dosis elevadas de los productos. Más recientemente Nicora et al. (2012) comprobaron efectos comparables en suelos de textura franco-arenosa del centro E de la provincia de Buenos Aires.
El aumento del pH del suelo puede acarrear algunos efectos secundarios, entre ellos la modificación de la estabilidad de los agregados edáficos. En suelos ácidos el incremento de pH disminuye las cargas variables positivas y con ellas podría disminuir la estabilidad estructural (Roth y Pavan, 1991). Albuquerque et al. (2003) demostraron que si bien ocurre un aumento de la dispersión de arcilla con la dosis de calcáreo en el caso de un suelo del planalto brasilero, el mayor aporte orgánico originado por el beneficio del encalado, compensa el proceso dispersivo, no alterándose en consecuencia la estabilidad estructural. Como puede verse, el fenómeno es multivariable y es necesario profundizar en estos procesos para diferentes ambientes edafo-climáticos. Otros autores, por el contrario, han puesto en evidencia una mejora en dicha propiedad, haciendo referencia a la formación de puentes cálcicos que favorecen la floculación de los coloides del suelo (Chan y Heenan, 1999). Las diferencias encontradas radican en las cargas dominantes de los coloides en cada tipo de suelo, las cuales están relacionadas con la mineralogía y acidez del mismo, por lo que no se puede hacer generalizaciones en este sentido.
Relacionado con la modificación de las propiedades físicas, Vázquez et al. (2009) encontraron que el agregado de caliza y dolomita modificó la resistencia a la penetración en forma variable según dosis/profundidad de evaluación en suelos del Pdo. de La Plata (Buenos Aires). Los autores destacaron que dosis bajas del orden de 1.000 kg ha-1 redujeron la resistencia respecto del testigo, afirmando su acción sobre la estructuración del suelo. Sin embargo, se advirtió que dosis más elevadas, 1.500 y 2.000 kg ha-1, por el contrario, aumentaban la resistencia respecto del testigo, argumentando que podría tratarse de recristalización de los carbonatos. Esta recristalización obturaría el espacio poroso en los suelos de textura fina y por ende con predominio de poros de tamaño pequeño. Estos resultados se asociaron con medidas biológicas (desarrollo de hongos y rendimiento de alfalfa), por lo que en suelos de texturas finas podrían ser desaconsejadas dosis elevadas de los productos. Más recientemente Nicora et al. (2012) comprobaron efectos comparables en suelos de textura franco-arenosa del centro E de la provincia de Buenos Aires.
Otro efecto secundario de esta práctica es la variación en la disponibilidad de nutrientes, al margen de los aportados por el encalado. Es ampliamente conocida la modificación de la solubilidad de los fosfatos con el incremento del pH. De la misma manera se comprobaron cambios en la disponibilidad de micronutrientes. Fernades Boaro et al. (1999) comprobaron menor disponibilidad de Cu, Zn y Mn en plantas de poroto sobre suelos encalados. Andreotti et al. (2001) afirmaron poder superar la deficiencia de Zn causada por el encalado de maíz, mediante fertilización con este elemento.
Uno de los efectos secundarios de mayor importancia es la reducción del Al soluble. A valores de pH 5,3-5,5 el Al forma Al(OH)3 precipitado y por debajo de dicho rango se forman especies solubles, capaces de ser intercambiadas (Al3+, Al(OH)2+, Al(OH2)+). Cuando el encalado permite superar aquel valor de pH, la toxicidad del elemento se reduce considerablemente. Esto es principalmente relevante en el noreste de nuestro país que posee suelos con mayor grado de desarrollo debido al clima subtropical y por ende, mayor acidez y factibilidad de toxicidad de Al. Si bien en el ámbito templado la concentración de Al soluble potencial es relativamente reducida, Millán et al. (2010) encontraron que el encalado disminuyó también la concentración de este elemento en el ámbito templado Argentino.
Uno de los efectos secundarios de mayor importancia es la reducción del Al soluble. A valores de pH 5,3-5,5 el Al forma Al(OH)3 precipitado y por debajo de dicho rango se forman especies solubles, capaces de ser intercambiadas (Al3+, Al(OH)2+, Al(OH2)+). Cuando el encalado permite superar aquel valor de pH, la toxicidad del elemento se reduce considerablemente. Esto es principalmente relevante en el noreste de nuestro país que posee suelos con mayor grado de desarrollo debido al clima subtropical y por ende, mayor acidez y factibilidad de toxicidad de Al. Si bien en el ámbito templado la concentración de Al soluble potencial es relativamente reducida, Millán et al. (2010) encontraron que el encalado disminuyó también la concentración de este elemento en el ámbito templado Argentino.
BIBLIOGRAFÍA
- Abruña, F. y J. Vicente. 1955. Requirement of a cuantitative method for determining the lime requirement of soil. Journal of Agric. of the University of Puerto Rico 39: 41 - 45.
- Adams, F., y C.E. Evans. 1962. A rapid method for measuring lime requirement of red-yellow podzolic soils. Soil Sci. Soc. Am. Proc. 26:355-357.
- Alburquerque, J.A., C. Bayer, P.R. Ernani, A.L. Mafra, y E.C. Fontana. 2003. Aplicação de calcário e fósforo e e estabilidade da estrutura de um solo ácido. Rev. Bras. Ciênc. Solo 27 (5): 799-806.
- Alcarde, J.C., y A.A. Rodella. 1996. O Equivalente em carbonato de cálcio dos corretivos da acidez dos solos. Sci. Agric. 53(2-3): 204 – 210.
- Amaral, A.S., I. Anghinoni, R. Hinrichs, y I. Bertol. 2004. Movimentação de partículas de calcário no perfil de um Cambissolo em plantio direto. Rev. Bras. Ciênc. Solo 28(2): 359 – 367.
- Anjos Reis, R., P.C. Rezende Fontes, J.C. Lima Neves, y N. Terra Santos. 1999. Total soil electrical conductivity and critical soil K+ to Ca2+ and Mg2+ ratio for potato crops. Soil Agric. 56(4): 993 – 997.
- Andreotti M., E. C. A. De Souza, y C.A. Costa Cruscio. 2001. Componentes morfológicos e produção de materia seca de milho em função da aplicação de calcário e zinco. Sci. Agric. 58(2): 321 – 327.
- Aranzazú Sucunza F., Pellegrini A., Vázquez M. 2014.Comparación de metodologías analíticas para el diagnóstico de la acidez y el complejo de cambio en suelos tratados con enmiendas básicas. Trabajo presentado al XXIV Congreso Argentino de la Ciencia del Suelo.
- Azcon Bieto, J., y M. Talon. 2008. Fundamentos de Fisiología Vegetal. Mc Graw Hill Ed. Madrid, España. ISBN 8448151682. 656 p.
- Balcaza, L. 1996. Fertirrigación en cultivos hortícolas. Boletín Hortícola FCAyF/UNLP, octubre, 7-9.
- Balcaza, L. 2003. Deterioro de los suelos cultivados bajo invernáculo. IDIA XXI, 4: 196-200.
- Barbieri, P. A., H.E. Echeverría, y H.R. Saínz Rozas. 2010. Soybean response to lime and micronutrients application in argentinean molisols. 102 American Society of Agronomy (ASA) annual meeting. 31 Octubre-3 Noviembre. Long Beach CA-USA. Actas CD 1 p.
- Bear, F.E., y S.J. Toth. 1948. Influence of Ca on availability of other soil cations. Soil Sci. 65: 69-75.
- Bell, P.F. 1996. Predicting liming needs of soybean using soil pH, aluminum and manganese soil test. Comm soil sci plant anal 27 (13-14): 2749-2764.
- Bennardi D., Díaz Gorostegui A. y M. Vázquez. 2014. Capacidad buffer edáfica de la Pradera Pampeana para tomar decisiones de encalado. Trabajo presentado al XXIV Congreso Argentino Ciencia del Suelo.
- Bhumbla, D.K., y E.O. Mc Lean. 1965. Aluminum in soils: VI. Changes in pH-dependent acidity, cation-exchange capacity, and extractable aluminum with additions of lime to acid surface soils. Soil Sci. Soc. Amer. Proc. 29: 370-374.
- Bianchini, A.A., y A.P. Mallarino. 2002. Soil-sampling alternatives and variable-rate liming for a soybean-corn rotation. Agron. J. 94:1355-1366.
- Borie, B.F., F.A. Gallardo, M.L.G. Mora, y J.C. García. 1999. Sensibilidad y tolerancia a la acidez de los cultivos en condiciones de campo. Frontera Agrícola 5 (1-2): 19 – 28.
- Büll, L.T., R.L. Villas Bôas, y J. Nakagawa. 1998. Variações no balanço catiônico do solo inducidas pela adubação potássica e efeitos na cultura do alho vernalizado. Sci. Agric. 55(3): 456-464.
- Caires, E.F., W.A. Chueiri, E.F. Madruga, y A. Fuigueiredo. 1998. Alterações químicas do solo e resposta da soja ao calcário e gesso aplicados na superfície em sistema de cultivo sem preparo do solo. Rev Bras Ciênc Solo 22: 27.
- Caires, E.F., J. Blum, G. Barth, F.J. Garbuio, y M.T. Kusman. 2003. Alterações químicas do solo e resposta da soja ao calcário e gesso aplicados na implantação do sistema plantio direto. Rev. Bras. Ciênc. Solo 27(2): 275.
- Carver, B., y Y J. Ownby. 1995. Acid soil tolerance in wheat. Adv Agron 54: 117-173.
- Chan K.Y., y D.P. Heenan. 1999. Lime-induced loss of soil organic carbon and effect on agrégate satability. Soil Sci. Soc. Am. J. 63: 1841-1844.
- Ciotta, M.N., C. Bayer, P.R. Ernani, S.M.V. Fontoura, C. Wobeto, y J.A. Albuquerque. 2004. Manejo da calagem e os components da acidez de Latossolo Bruno em plantio direto. Rev. Brás. Ciênc. Solo 28(2): 317 – 326.
- Cochrane, T., J. Salinas, y P. Sánchez. 1980. An equqtion for liming acid mineral soils to compesate crops aluminium tolerance. Trop. Agr. 57 (2): 133-140.
- Culot, J. 1967. Condiciones edáficas relacionadas con la hipomagnesemia del ganado en el SE bonaerense. INTA. Balcarce. Boletín Técnico Nº51.
- Darwich, N. 2006. Los nutrientes secundarios: azufre, calcio y magnesio. En Manual de Fertilidad de Suelos y uso de Fertilizantes. Cap. VII, p. 131-150. 3º Edición. Fertilizar Asoc. Civil, Mar del Plata. ISBN 987-43-9313-0. 289 p.
- Demanet, R.F., B.M. Schnettler, y M.L.G. Mora. 1999. Efecto del encalado y su relación con los nutrientes sobre la producción de pasturas en suelos ácidos. Frontera Agrícola 5 (1-2): 95-110.
- Dietzel, K.A., Q.M. Ketterings, y R. Rao. 2009. Predictions of lime needs for pH and aluminium management of New York agricultural soils. Soil Sci. Soc. Am. J. 73:443-448.
- Estelrrich, C; Ossola, J; Juan, L; Vázquez, M; Millán, G. 2012. Efecto de la fertilización nitrogenada sobre el pH en dos suelos de la Pradera Pampeana. XIX Congreso Latinoamericano y XXIII Congreso Argentino de la Ciencia del Suelo, abril, Mar del Plata, Argentina.
- Farina, M.P.W., P. Channon, y G.R. Thibaud. 2000. A comparation of strategies for ameliorating subsoil acidity: I. Long-term growth effects. Soil Sci. Soc. Am. J. 61: 646-651.
- Fernández Boaro C.S., J.A. Proença Vieira De Moraes, J.D. Rodríguez, E.O. Onol, y P.R. Curi. 1999. Interações entre magnesio e micronutrientes metálicos durante o desenvolvimento de feijoeiro, en solução nutritiva. Sci. Agric. 56 (1): 125-134.
- Gambaudo, S., L. Picco, P. Soldano, y A. Cervetti. 2007. Fertilización compuesta con calico, magnesio y azufre en soja. Resultados experiencias campaña 2006/07. INTA. EEA Rafaela. Información Técnica cultivos de verano. Publicación Miscelánea Nº108.
- García, M., y M. Vázquez. 2011. Impacto de la evolución de la agricultura santafesina en la pérdida de nutrientes básicos de los suelos. Valoración económico-ecológica. V Congreso Iberoamericano sobre Desarrollo y Ambiente/V Jornada de la Asociación Argentino Uruguaya de Economía Ecológica. Universidad Nacional del Litoral de Sta Fe, 9/2011.
- González, B., S. Gambaudo, D. Bersano, D. Tenorio, J. Neifert, y D. Osenda. 2001. Enmiendas en trigo. Fertilizar 6(23): 18-19.
- Havlin, J.L., J.D. Beaton, S.L. Tisdale, y W.L. Nelson. 2005. Soil acidity and alkalinity. En J.L. Havlin, J.D. Beaton, S.L. Tisdale, W.L. Nelson (ed.) Soil fertility and fertilizers. Pearson Prentice Hall. New Jersey. 7th ed, p. 45-96.
- Järvan, M. 2004. Available plant nutrients in growth substrate depending on various lime materials used for neutralizing bog peat. Agronomy Research 2(1): 29-37.
- Järvan, M., y P. Põldma. 2004. Content of plant nutrients in vegetables depending on various lime materials used for neutralising bog peat. Agronomy Research 2(1): 39-48.
- Kamprath, E.J. 1984. Crop response to lime on soils in the tropic. En Soil acidity and liming: 349-368. Ed. F. Adams. Am. Soc. Agronomy, Wisconsin, EEUU.
- Kissel, D.E., R.A. Isaac, R. Hitchcock, L.S. Sonon, y P.F. Vendrell. 2007. Implementation of soil lime requirement by a single-addition titration method. Commun. Soil Sci. Plant Anal. 38:1341-1352.
- Kollmeier, M., H.H. Felle, y W.J. HORST. 2000. Genotypical differences in aluminum resistance of maize are expressed in the distal part of the transition zone. Is reduce basi-petalauxin flow involved in inhibition of root elongation by aluminum? Plant Physiol. 122 (3) 945-956.
- Liu, M., D.E. Kissel, M.L. Cabrera, y P.F. Vendrell. 2005. Soil lime requirement by direct titration with a single addition of calcium hydroxide. Soil Sci. Soc. Am. J. 69: 522-530.
- Loide, V. 2004. About the effect of the contents and ratios of soil's available calcium, potassium and magnesium in liming of acid soils. Agron. Res. 2(1): 71-82.
- Martínez, F., y G. Cordone. 2008. Soja 2008. Para Mejorar la Producción/39 Estación Experimental Agropecuaria Oliveros Centro Regional Santa Fe" ISSN 1850-163X p. 78-80.
- Mc Lean, E.O., D.J. Eckert, G.Y. Reddy, y F.J. Trierweiler. 1978. An improved SMP soil lime requirement method incorporating double-buffer and quick-test features. Soil Sci. Soc. Am. J. 42: 311-316.
- Melgar, R., J. Lavandera, y M.E. Camozzi. 1999. Fertilización balanceada, clave para la alta productividad. Fertilizar 17: 24-25. INTA. Argentina.
- Mehlich, A. 1976. New buffer pH method for rapid estimation of TA and lime requirement of soils. Commun. Soil Sci. Plant Anal. 7: 637-652.
- Mengel, K., y E.A. Kirkby. 2000. Principios de Nutrición Vegetal. Cap.11: 401 – 423, Cap 12: 425 – 434. Ed. Instituto Internacional de la Potasa, Basilea, Suiza. 607 p. Merani V., Larrieu L., Ossola J., Vázquez M., Santa María M., Rojas M., Pelatti V., Millán G., Esterlich C. Y L. Juan. 2014. Efecto de la fertilización nitrogenada sobre el pH del suelo con y sin siembra de Lolium multiflorum. Trabajo presentado al XXIV Congreso Argentino de la Ciencia del Suelo, 5-9 de mayo. Bahía Blanca.
- Millán, G., M. Vázquez, A. Terminiello, y D. Santos Sbuscio. 2010. Efecto de las enmiendas básicas sobre el complejo de cambio en algunos suelos ácidos de la región pampeana. Ciencia del Suelo 28(2): 131-140.
- Miller, R.O., and D.E. Kissel. 2010. Comparisons of soil pH methods on soils of North America. Soil Sci. Soc. Am. J. 74: 310-316.
- Moseley, G., y D.H. Baker.1991. The efficacy of a high magnesium grass cultivar in controlling hypomagnesaemia in grazing animals. Grass Forage Sci. 46: 375-380.
- Muñoz Hernández, R.J., y R.I. Silveira. 1998. Efeitos da saturação por bases, relações Ca:Mg no solo e níveis de fósforo sobre a produção de material seco e nutrição mineral do milho (Zea mays L.). Sci. Agric. 55(1): 79-85.
- Nicora, Z., F. Guilino, A. Terminiello, G. Millán, y M. Vázquez. 2012. Efecto del Encalado sobre la Resistencia Mecánica de un Hapludol Éntico Bonaerense. XIX Congreso Latinoamericano y XXIII Congreso Argentino de la Ciencia del Suelo. 16-20/5/2012. Mar del Plata, Argentina.
- Oliveira, E.L. 1993. Rendimento de matéria seca e absorção de cálcio e magnesio pelo milho em função da relação cálcio/magnesio no solo. Ver. Bras. Ciênc. Solo 17: 383-388.
- Oliveira, E.L., y M.S. Parra. 2003. Resposta do feijoeiro a relações variáveis entre cálcio e magnesio na capacidade de troca de cátions de latossolos. Rev. Bras. Ciênc. Solo 27 (5): 859-866.
- Pagani, A., A.P. Mallarino, y J.E. Sawyer. 2009. Soil pH and lime management for corn and soybean: an ongoing on-farm project. North Central Extension-Industry Soil Fertility Conference. November 18, 2009. Des Moines, IA. p. 106-112. Pagani, A., and A.P. Mallarino. 2011. Comparison of soil pH measured in water and calcium chloride to predict crop response to lime in Iowa. Agronomy Abstracts. CD-ROM. ASA-CSSA-SSSA. Madison, WI.
- Pagani, A., and A.P. Mallarino. 2012. Comparison of methods to determine crop lime requirement under field conditions. Soil Sci. Soc. Am. J. 76:1855–1866.
- Piaggio, D., y W. Costa. 1996. Fertirriego en tomate y pimiento. Fertilizar 4: 16-17. INTA. Argentina.
- Pierce, F.J., y D.D. WARNKE. 2000. Soil and crop response to variable-rate liming for two Michigan Fields. Soil Sci. Soc. Am. J. 64: 774-780.
- Pooviah, B.W., y A.S.N. Reddy. 1996. Calcium and geotropism. En Y. Waisel et al. Ed. Plants rotos: The hidden half. Academis Press. New York. p. 307-321.
- Porta, J., M. López Acevedo, y C. Roquero. 1999. Edafología para la Agricultura y el Medio Ambiente Cap. 10: 217-236. 2º Ed. Ediciones Mundi Prensa, Madrid. 849 p.
- Richter, M., M. Conti, y G. Maccarini. 1982. Mejoras en la determinación de cationes intercambiables, ácidos intercambiables y capacidad de intercambio catiónica en suelos. Rev. Fac. Agronomía 3 (2): 145-155.
- Romheld, V., y M. El-Fouly. 2001. Fertilización foliar, una vía no tradicional. Fertilizar 24: 30-34. INTA, Argentina.
- Roth, C.H., y M.A. Pavan. 1991. Effects of lime and gypsum on clay dispertion and infiltration in samples of Brazilian Oxisol. Geoderma 48: 351-361.
- Sadzawka A.R., Carrasco M., Grez R., Mora M., Flores H. y A. Neaman. 2006. Métodos de análisis recomendados para los suelos de Chile. Serie Actas INIA Nº34. Chile.
- Shoemaker H.E., O. Mc Lean y P.F. Pratt. 1961. Buffer method for determining lime requirement of soil with apreciable amount of extractable aluminium. Soil Sci. Am. Proc. 25: 274-277.
- Sikora, F.J. 2006. A buffer that mimics the SMP buffer for determining lime requirement of soil. Soil Sci. Soc. Am. J. 70: 474-486.
- Silva, H., y P. Larraín. 1997. Manzanos: fertilizantes foliares cálcicos en desórdenes fisiológicos. Fertilizar 9: 16-19. INTA. Argentina.
- Sims, J. T. 1996. Lime requirement. In: D.L. Sparks, editor, Methods of soil analysis. Part 3. Soil Science Society of America Book Series No. 5. SSSA. Madison, WI. p. 491-515.
- Vázquez, M., A. Piro, G. Millán, y J. Lanfranco. 2002. Pautas para erl diagnóstico de la problemática asociada a suelos ácidos de zonas templadas subhúmedas. Revista de la Asociación Argentina de la Producción Animal 23(2).
- Vázquez M., Rotondaro R. 2005. Acidificación de suelos en el sur de Santa Fe y el norte bonaerense. Revista de la Asociación de Cooperativas Argentinas Acaecer 350: 26 – 32.
- Vázquez, M., A. Terminiello, y G. Millán. 2008. Lixiviación de iones en un suelo tratado con enmiendas carbonáticas y yeso. XXI Congreso Argentino de la Ciencia del Suelo. 16/5/08, Potrero de Funes, San Luis. ACTAS: 342. Trabajo completo versión electrónica.
- Vázquez, M., A. Terminiello, A. Duhour, M. García, y F. Guilino. 2009. Efecto de correctores de acidez sobre las propiedades físicas de un Argiudol típico de la pradera pampeana. Revista de la Asociación Argentina de la Ciencia del Suelo 27 (1):67-76.
- Vázquez, M., A. Terminiello, A. Casciani, G. Millán, P. Gelati, F. Guilino, J. García Díaz, J. Kostiria, y M. García. 2010. Influencia del agregado de enmiendas básicas sobre la producción de alfalfa (Medicago sativa l.) en ámbitos templados argentinos. Ciencia del Suelo 28 (2): 141-154.
- Vázquez, M., A. Terminiello, A. Casciani, G. Millán, D. Cánova, P. Gelati, F. Guilino, A. Dorronzoro, Z. Nicora, L. Lamarche, y M. García. 2012.Respuesta de la soja (glicine max l.merr) a enmiendas básicas en algunos suelos de las provincias de Buenos Aires y Santa Fe. Ciencia del Suelo 30(1): 43-55.
- Vigil, A. 2002. Viñedos. Fertilizar, diciembre: 18-22. INTA, Argentina.
- Villagarcia, MR., T.E. Carter, JR., T.W. Ruffy, A.S. Niewoehner, M.W. Jennnette, y C. Arellano. 2001. Genotipyc ranking for aluminium tolerance of soybean root grown I hidroponics and sand cultura. Crops Sci; 412: 1499-1507.
- Vivas, H. S., H. Fontanetto, y R. Albrecht. 2001. Fertilizacion con calcio, magnesio y azufre sobre la produccion de maiz en dos sitios del centro de Santa Fe. Información Técnica
- de Cultivos de Verano. Estación Experimental Agropecuaria Rafaela, INTA. Publicación Miscelánea Nº 95, Nº 4: 1-5.
- Vivas, H., y H. Fontanetto. 2003. Fósforo, azufre y calcio en la producción de soja en el Departamento San Justo. 2002/2003. INTA, Estación Experimental Agropecuaria Rafaela. Información Técnica de cultivos de verano. Campaña 2003. Publicación Miscelánea Nº100, Nº15, 5 p.
- Weisz, R., J. White, B. Knox, y L. Reed. 2003. Long-term variable rate lime and phosphorus application for Piedmont no-till field crops. Precision Agric 4(3): 311-330.
- Widmann, G. 2002. Naranjos. Fertilizar, diciembre: 15-17. INTA. Argentina.
- Woodruff, C.M. 1948. Testing soils for lime requirement by means of a buffered solution and the glass electrode. Soil Sci. 66: 53-63.
- Yuan, T.L. 1974. A double buffer method for the determination of lime requirement of acid soil. Soil Sci. Soc. Am. J. 38: 437-440.
- Zalewska, M. 2003. The efect of varios calcium, magnesium, potasium and hidrogen saturation of CEC on the yield and mineral composition of yelow lupine. Pol. J. Natur. Sc. 15 (3): 321-334.
- Zalewska, M. 2005. The efect of varios calcium, magnesium, potasium and hidrogen saturation of CEC on the yield and mineral composition of oat. J. Elementology 10 (4): 1137-1148.
- Zalewska, M. 2008. The efect of varios calcium, magnesium, potasium and hidrogen saturation of CEC on the yield and mineral composition of sunflower. Pol. J. Natur. Sc. 23 (2): 347-365.
FUENTE: ENGORMIX